Ya puedes escuchar el podcast de mi sección Eureka en La Rosa de los Vientos de Onda Cero. Como siempre una transcripción, algunas imágenes y algunos enlaces.
Desde hace muchos años se habla de la medicina regenerativa: El uso de las células madre para curar órganos enfermos o dañados, y revertir enfermedades incurables. Este mes ha sido noticia que un trasplante de células madre a devuelto la visión a personas ciegas. ¿Qué es exactamente lo que se ha logrado? Las células madre embrionarias, cuyo nombre más correcto es células troncales pluripotentes, son capaces de convertirse en cualquier célula de cualquier tejido del cuerpo humano. Desde los trabajos en 1981 en células madre de ratones realizados por el galés Martin Evans, Premio Nobel de Medicina en 2007, y en 1998 en células madre humanas realizados por el estadounidense James Thomson, se habla de su gran potencial en medicina para regenerar órganos, como corazones infartados, hígados diabéticos, cerebros con ictus, párkinson, alzhéimer, etc. Más aún tras el descubrimiento de que se pueden reprogramar células adultas para convertirlas en células pluripotentes, que fue premiado con el Premio Nobel de Medicina de 2012 para el japonés Shinya Yamanaka. Sin embargo, hacer realidad este deseo ha resultado mucho más difícil de lo esperado. Este mes ha sido noticia un artículo liderado por Robert Lanza, profesor de la Universidad Wake Forest, Carolina del Norte, que trabaja para la empresa biotecnológica ACT (Advanced Cell Technology), que ha sido elegido por la revista Time como una de las 100 personas más influyentes del mundo en 2014. Lanza y sus colegas han publicado en la prestigiosa revista de medicina The Lancet los resultados tras tres años de seguimiento de 18 pacientes en EE UU que recibieron un injerto de células madre en la retina de uno de sus ojos. Tras tres años de la operación de cirugía no ha causado efectos secundarios graves, ni tumores, ni rechazo. Los resultados han sido espectaculares, aunque se trataba de un estudio de fase 1, centrado en la bioseguridad del tratamiento.
Más información divulgativa (de corte optimista) en Nuño Domínguez, «Un trasplante de células madre devuelve la visión a personas ciegas,» El País, Materia.es, 15 Oct 2014; «Las células madre adultas demuestran que pueden regenerar un órgano humano dañado,» Materia.es, 06 Jul 2014; Blue Sky Science, «Stem cell therapy allows blind to see again, thanks to animal research,» Speaking of Research, 15 Oct 2014. Más realistas son Antonio Regalado, «Stem Cells Seem Safe in Treating Eye Disease,» MIT Tech Review, 14 Oct 2014; Paul Knoepfler, «Encouraging New Paper on ACT Stem Cell-Based Trial for Macular Degeneration,» iPS Cell, 14 Oct 2014.
El artículo técnico es Steven D. Schwartz et al., «Human embryonic stem cell-derived retinal pigment epithelium in patients with age-related macular degeneration and Stargardt’s macular dystrophy: follow-up of two open-label phase 1/2 studies,» The Lancet, AOP 15 Oct 2014 [PDF gratis]; Steven D. Schwartz et al., «Embryonic stem cell trials for macular degeneration: a preliminary report,» The Lancet 379: 713-720, 25 Feb 2012 [PDF gratis].
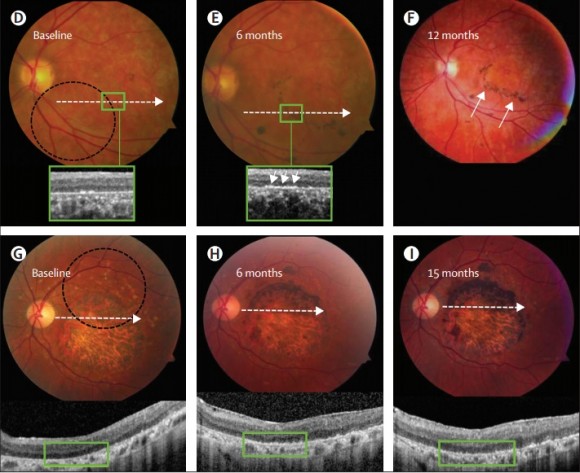
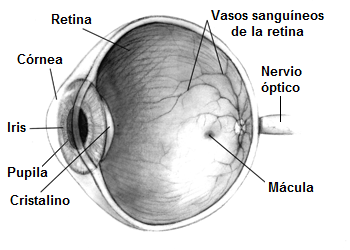
El injerto de células madre en la retina de 18 personas ciegas les ha devuelto parcialmente la visión. ¿Podría aplicarse la técnica a cualquier persona ciega o hay algún tipo de restricción? Los 18 pacientes que han recuperado o mejorado su visión padecían dos enfermedades concretas de la retina que afectan a la mácula, la zona central de la retina que permite la visión fina de los detalles. Estas dos enfermedades de la retina son la causa más común de ceguera entre jóvenes y adultos en los países desarrollados. Nueve de los pacientes sufrían la enfermedad de Stargardt, una enfermedad hereditaria cuyos síntomas suelen empezar en la adolescencia, que provoca una pérdida de agudeza visual progresiva; estos pacientes tenían entre 20 y 71 años. Y los otros nueve pacientes padecían degeneración macular asociada a la edad, una enfermedad propia de la vejez; estos pacientes tenían entre 70 y 88 años. Ambas enfermedades afectan a la mácula lútea, una capa amarillenta de tejido sensible a la luz que se encuentra en la parte posterior del ojo, en el centro de la retina. La mácula proporciona la agudeza visual, la que permite al ojo percibir detalles finos y pequeños, lo que nos sirve para poder leer y distinguir las caras de las personas. Robert Lanza y sus colegas han implantado en el epitelio pigmentario retinal (conocido como EPR) de uno de los dos ojos de cada paciente células cultivadas en laboratorio a partir de células pluripotentes. De los 18 pacientes tratados, diez experimentaron mejoras en la visión, siete mejoraron moderadamente o quedaron estables y uno sufrió pérdida de visión. Los ojos no tratados no mejoraron en estos pacientes.
No todos los pacientes han recuperado completamente la visión, aunque la han mejorado de forma espectacular. Podemos decir que el principal mensaje de este estudio es que hay esperanza para muchos enfermos. ¿Cuándo estarán disponibles futuros tratamientos? Lo primero que debo decir es que no debemos dar falsas esperanzas a los enfermos que sufran la enfermedad de Stargardt o la degeneración macular. Los ensayos en ratas y ratones han dado resultados muy prometedores desde el año 2003, pero este primer ensayo en humanos es de fase 1/2 y los resultados con 18 pacientes no son aún estadísticamente significativos. Hay que recordar que los ensayos de fase 1 son ensayos de bioseguridad y se suelen realizar con pacientes sanos. En este caso, como la intervención requiere cirugía y tenemos dos ojos, se ha aplicado a uno de los ojos de pacientes enfermos, algo propio de un ensayo de fase 2. Aún así, el foco del estudio se ha centrado en la seguridad del tratamiento, sobre todo, descartar el riesgo de que se produzcan tumores (teratomas) provocados por las células transplantadas que tienen memoria de su origen, así como evitar el riesgo de rechazo. Los pacientes se han dividido en tres grupos de seis, tres con cada enfermedad, cada grupo ha recibido un implante de 50 mil, 100 mil y 150 mil células. Hay que recordar que el epitelio pigmentario retinal humano tiene entre 4,5 y 6 millones de células. Serán necesarios futuros estudios de fase 2 para determinar cuántas células hay que implantar para lograr un tratamiento óptimo. Robert Lanza ha dicho que su empresa ACT quiere recabar una inversión de 10 millones de dólares para iniciar ensayos de fase 2 a final de este año. Si todo sale bien en futuros ensayos los trasplantes podrían estar en uso clínico a gran escala en unos diez años, como muy pronto. Hay mucho interés industrial en comercializar los tratamientos con células madre cuanto antes, pero hay que tener muy presente que se trata de un proceso lento.
Recomiendo leer a Anthony Atala, «Human stem cell-derived retinal cells for macular diseases,» The Lancet, AOP, 15 Oct 2014.
Este estudio podría dar la luz verde hacia otras aplicaciones de las células madre en enfermedades incurables como el alzhéimer o muy frecuentes como la diabetes o los problemas cardiovasculares. ¿Cómo se encuentra la situación actual en medicina regenerativa? El Premio Nobel de Medicina de 2012 concedido a Shinya Yamanaka por las técnicas de reprogramación de células adultas de un paciente hasta células madre, las llamadas células pluripotentes inducidas o iPS, tan versátiles como las células madre embrionarias, pero que no despiertan recelos éticos porque no exigen destruir un embrión, y que prometen evitar el riesgo de rechazo, ha hecho que varios países, sobre todo Japón y EEUU, hayan realizado importantes inversiones en el campo de la medicina regenerativa. Sin embargo, la mayoría de los estudios se centran en la retina y en la degeneración macular porque su naturaleza «inmunoprivilegiada» y su capacidad de tolerar células extrañas sin provocar una fuerte respuesta inmunitaria. Por ejemplo, en septiembre de este año en Japón, un equipo médico del Instituto Riken, implantó por primera vez en el mundo células iPS humanas en una paciente de 70 años que sufre una grave degeneración macular asociada a la edad. También se ha solicitado permiso para los primeros ensayos en el tratamiento de la insuficiencia cardíaca. Sin embargo, se trata de estudios de fase 1, es decir, para evaluar la seguridad de la técnica. Los estudios de fase 2 tardarán en llegar. Se requiere un gran número pacientes para evaluar el valor clínico de un tratamiento. No debemos ofrecer falsas esperanzas. La efectividad de los tratamientos con células madre requerirá décadas de investigación.
Más información, por ejemplo, en Maribel Marín, «Japón realiza el primer trasplante en humanos de células iPS,» El País, 12 Sep 2014.