
Hoy se ha publicado un artículo de The Lancet con los resultados del ensayo de fase 1/2 de la vacuna contra el SARS-CoV-2 del Instituto Gamaleya de Investigación en Epidemiología y Microbiología en Moscú, Rusia. Aunque se ha aprobado su uso por motivos políticos(⋇), hasta que no supere los ensayos de fase 3 no se sabrá si es efectiva para la población general. En el ensayo de fase 1/2 con 38 voluntarios para cada tipo de vacuna (Gam-COVID-Vac y Gam-COVID-Vac-Lyo) los efectos adversos de la vacuna fueron leves (similares a los de un resfriado, luego tratables con analgésicos). Además, se observó una buena respuesta inmunogénica en los ensayos ELISA (ensayo por inmunoabsorción ligado a enzimas), tanto respuesta humoral (generación de anticuerpos IgG a los 14 días con un máximo a los 28 días), como respuesta celular (proliferación de linfocitos CD4 y CD8, y medidas del interferón-γ, ambos en cultivo). En líneas generales son resultados similares a los de otras vacunas que ya han publicado los resultados de sus ensayos de fase 1/2.
Como ya indiqué en este blog, la vacuna vehicula el gen de la proteína espicular (S) del coronavirus usando virus de ADN que producen resfriados (adenovirus recombinantes humanos de tipo 5 y 26). Hay dos versiones de la vacuna, una líquida Gam-COVID-Vac, que requiere cadena de frío, y otra seca Gam-COVID-Vac-Lyo, que no la requiere. Ambas se han probado en sendos grupos de 38 (=9+9+20) voluntarios sanos de entre 18 y 60 años (53 hombres y 23 mujeres), luego no es un ensayo aleatorizado. Los ensayos de fase 1 (seguridad entre 0 y 28 días) de rAd26 y rAd25 se probaron en sendos grupos de 9 voluntarios, y los de fase 2 (eficacia y seguridad entre 0 y 42 días) en los restantes 20 voluntarios (primero vacunados con rAd26 y luego con rAd5). Los síntomas leves observados fueron: dolor en el lugar de la inyección (44 [58%]), fiebre (38 [50%]), dolor de cabeza (32 [42%]), astenia (21 [28%]) y dolores musculares y articulares (18 [24%]). En la fase 2, el 85 % de los participantes tenían anticuerpos detectables a los 14 días después de la dosis inicial, aumentando al 100 % el día 21, con aumento sustancial de los títulos tras la dosis de refuerzo.
Con solo los resultados del ensayo de fase 1/2 solo podemos decir que es una vacuna tan prometedora como las demás que ya han publicado sus resultados de esta fase; no se puede afirmar que ninguna de las vacunas que han iniciado su fase 3 sea mejor o peor que las demás; hasta que no se supere dicha fase es imposible saberlo. El artículo es Denis Y Logunov, Inna V Dolzhikova, Alexander L Gintsburg, «Safety and immunogenicity of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine in two formulations: two open, non-randomised phase 1/2 studies from Russia,» The Lancet (04 Sep 2020), doi: https://doi.org/10.1016/S0140-6736(20)31866-3; un resumen divulgativo en Naor Bar-Zeev, «COVID-19 vaccines: early success and remaining challenges,» The Lancet (04 Sep 2020), doi: https://doi.org/10.1016/S0140-6736(20)31867-5.
[PS 08 sep 2020] (⋇) La autorización de la vacuna rusa viene con «trampa», pues en realidad se cambió la legislación rusa en abril para que la «autorización condicional para uso compasivo» pasara a llamarse «autorización» a secas, al menos en tiempos de pandemia. Nos lo cuenta María Jesús Lamas Díaz (Directora de la AEMPS) en su charla «La responsabilidad de la AEMPS como evaluadora de las vacunas y medicamentos para el tratamiento de la covid-19,» en el curso UIMP «XX Encuentro de la Industria Farmacéutica Española. El papel de la Industria Farmacéutica ante la pandemia del SARS CoV-2 · IV [UIMP TV min 14:30]. [/PS]

Lo más relevante de la inmunogénesis de las vacunas es la respuesta celular medida en cultivo de células mononucleares. Esta figura muestra los resultados de fase 1 (A, C y E) y de fase 2 (B, D y F) para la respuesta inmune celular en cultivo los días 0, 14 y 28 para linfocitos T colaboradores CD4+ (A y B), linfocitos T citotóxicos CD8+ (C y D) y para títulos (concentración) de inteferón-gamma IFNγ (E y F). Se detectó respuesta en todos los participantes el día 28, con una mediana de proliferación celular de 2.5 % para CD4+ y de 1.3 % para CD8+ con la vacuna congelada (Gam-COVID-Vac), y una mediana de proliferación celular de 1.3 % para CD4+ y de 1.1 % para CD8+ con la vacuna liofilizada (Gam-COVID-Vac-Lyo). La secreción de interferón-γ también aumentó mucho, en especial para las muestras de voluntarios de la fase 2. El artículo incluye un apéndice con tablas detalladas con todos los porcentajes de interés para evaluar estas respuestas [PDF, pp 16–21].
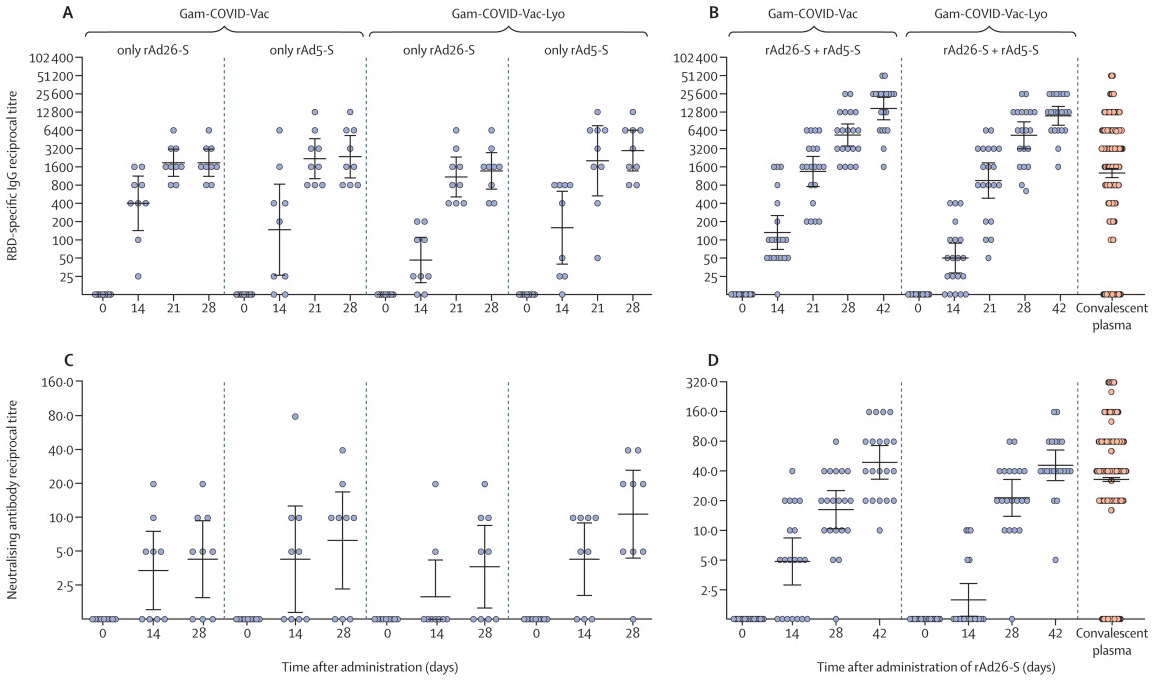
Esta figura muestra los resultados para la respuesta humoral para los estudios de fase 1 (A y C), los días 0, 14 y 28, y de fase 2 (B y D), los días 0, 14, 28 y 42, para los títulos (concentración) de anticuerpos IgG (A y B) y anticuerpos neutralizantes (C y D); estos últimos tienen como dianas el dominio de unión al receptor de la proteína espicular (S1 RBD), el dominio terminal de la subunidad S1 de dicha proteína (S1 NTD) o la segunda subnidad (S2), así bloquean la unión del coronavirus a la célula hospedadora y previenen la infección. Sin entrar en los detalles mostrados en la figura, se observa claramente en los datos del ensayo de fase 2 que la segunda dosis de refuerzo de la vacuna (con rAd5), a los 21 días de la primera dosis (con rAd26) logra un importante incremento de los títulos de IgG tras 7 días; en concreto, desde 1629 hasta 3442 para Gam-COVID-Vac (valor p <0.0001 el día 28 frente al día 21) y desde 951 hasta 5322 para Gam-COVID-Vac-Lyo (valor p < 0.0001 el día 28 frente al día 21). El día 42, los títulos de IgG fueron 14 703 para Gam-COVID-Vac y 11 143 para Gam-COVID-Vac-Lyo (figura 2).
Para entender estos resultados hay que compararlos con los ya publicados para otras vacunas (Oxford/AstraZeneca, CanSino y Moderna/NIH, entre otras). Sin entrar en detalles, los resultados de sus ensayos de fase 1/2 son muy similares (aunque la respuesta inmune celular se presenta de un modo diferente para cada una lo que impide una comparación rigurosa). Así que, en base solo a estos ensayos, con una duración de entre uno y dos meses, no se puede saber cuál es más prometedora para la fase 3, ya en curso en todas ellas (recuerda que la vacuna de Gamaleya haya sido aprobada por el gobierno ruso no significa nada desde un punto de vista científico). Hay que esperar a que se publiquen los resultados de los correspondientes ensayos de fase (con una duración de al menos un año). Habrá que esperar a finales de año para los primeros resultados preliminares tras seis meses y a mediados del año próximo para los resultados definitivos tras un año. Aún así, no hay que perder la esperanza de que para mediados del año 2021 haya vacunas disponibles en el mercado para el público de alto riesgo y que a finales de 2021 las haya para un público más general; a pesar de que no serán las mejores vacunas posibles, su impacto será muy relevante.


He leído con mucho interés la valoración que se hace en este blog acerca de la vacuna rusa frente al Sars CoV 2. Es posible que cualquier otro prototipo vacunal hubiera sido igualmente bien ponderado, porque a estos niveles de ensayo todos van muy bien, como no puede ser de otra forma. La respuesta inmune a la proteína S del coronavirus, bien se vehicule en un vector adenoviral, bien en un vector vaccinial o bien metida en liposomas, al final va a ser parecida. Parecida a este nivel básico de respuesta inmune elemental. La que se mide «in vitro» con la cuantificación de inmunoglobilinas, lifocitos T activados y diversas sustancias inmunotrópicas. Pero la verdadera efectividad de las vacunas hay que valorarla en el campo de batalla. Pero, según el autor del escrito «habrá que esperar a finales de año para los primeros resultados preliminares y a la primavera del año próximo para los resultados definitivos. Aún así, no hay que perder la esperanza de que para mediados del año 2021 haya vacunas disponibles en el mercado para el público de alto riesgo y que a finales de 2021 la haya para un público más general». Cuán largo me lo fiáis, que se dice que dijo cierto caballero andante. Y es que en esta ya larga saga del coronavirus, nada de lo que hoy se diga es sustentable en los días por venir. Quizá el virus se atenúe. Quizá se consiga una débil pero suficientemente solvente inmunidad grupal. Quizá todo sólo haya sido un mal sueño y en 2021 podamos decir: «¿ Hay vacunas?. Demasiado tarde. Ya todos nos inmunizamos».
«con aumento sustancial de los títulos tras la dosis de refuerzo»
La traducción de ‘titer’ o ‘titre’ es ‘concentración’, no ‘título’.
Hola Antonio, es perfectamente válido y habitual usar «titulación de anticuerpos» en el contexto en que lo ha usado Francis.
Un saludo
Cierto, Antonio, pero se usa mucho el anglicismo entre los expertos españoles, como bien sabrás.
Historia real.
Ingeniería industrial, primera práctica de termodinámica, exámen de práctica de aula (una mini-pregunta antes de empezar, para asegurarse de que el alumno ha leído el cuadernillo):
P: «Qué es el título»
R: «Estudio de la Ley de Gas-Lussac» (o algo por el estilo)
…
El primer cero de mi vida.
Vacuna probada solo en n=76 personas. ni siquiera es un ensayo II b…
Muy buen articulo , Dr.Villatoro, sin sordina.