
Ya puedes disfrutar del episodio 14 del podcast Biosíntesis [iVoox, iTunes, Google podcasts, Spotify, TuneIn, Radio Public]. El episodio fue grabado el viernes 30 de octubre de 2020, pero no se ha publicado hasta ayer 23 de junio de 2021; fue grabado usando Microsoft Teams y Zoom, así que pedimos perdón porque la calidad del audio no es óptima. Hemos cambiado un poco el formato y pretendemos que su duración máxima sea de 90 minutos. Como siempre presentamos artículos científicos y noticias sobre bioquímica y biología molecular. Participamos Silvana Tapia @SilvanaTapia3 (Dep. Microbiología , UMA), Belén Delgado Martín, @bio_Belen (estudiante de un Máster en Bioquímica, UMA), José (Pepe) Lozano @leviaingenia (Dep. Biología Molecular y Bioquímica, UMA), Íker Puerto San Román, @SrMitocondrio (estudiante del Grado de Bioquímica, UMA), autor del blog La Mitocondria, y un servidor, Francisco R. (Francis) Villatoro, @emulenews (Dep. Lenguajes y Ciencias de la Computación, UMA).
Ir a descargar el episodio BS14.

Pepe nos presenta un artículo de Joan Seaone (Hospital Universitario de Vall d’Hebron, Barcelona, España) y varios colegas que estudia el meduloblastoma, el tumor cerebral pediátrico más común. Caracterizar estos tumores es muy difícil porque se encuentran muy profundos en el encéfalo y solo se puede acceder a ellos con una intervención quirúrgica. Hace unos años se pensó que las biopsias líquidas eran la solución, pues permitirían ver el ADN del tumor en el sangre; por desgracia no se puede usar para este tipo de tumores. La propuesta del grupo de Seaone es usar el líquido cefalorraquídeo para estudiar el ADN de estos tumores (el llamado ctDNA, o ADN circulante tumoral); en el líquido cefalorraquídeo hay mayor concentración de ADN lo que facilita la biopsia de estos tumores.
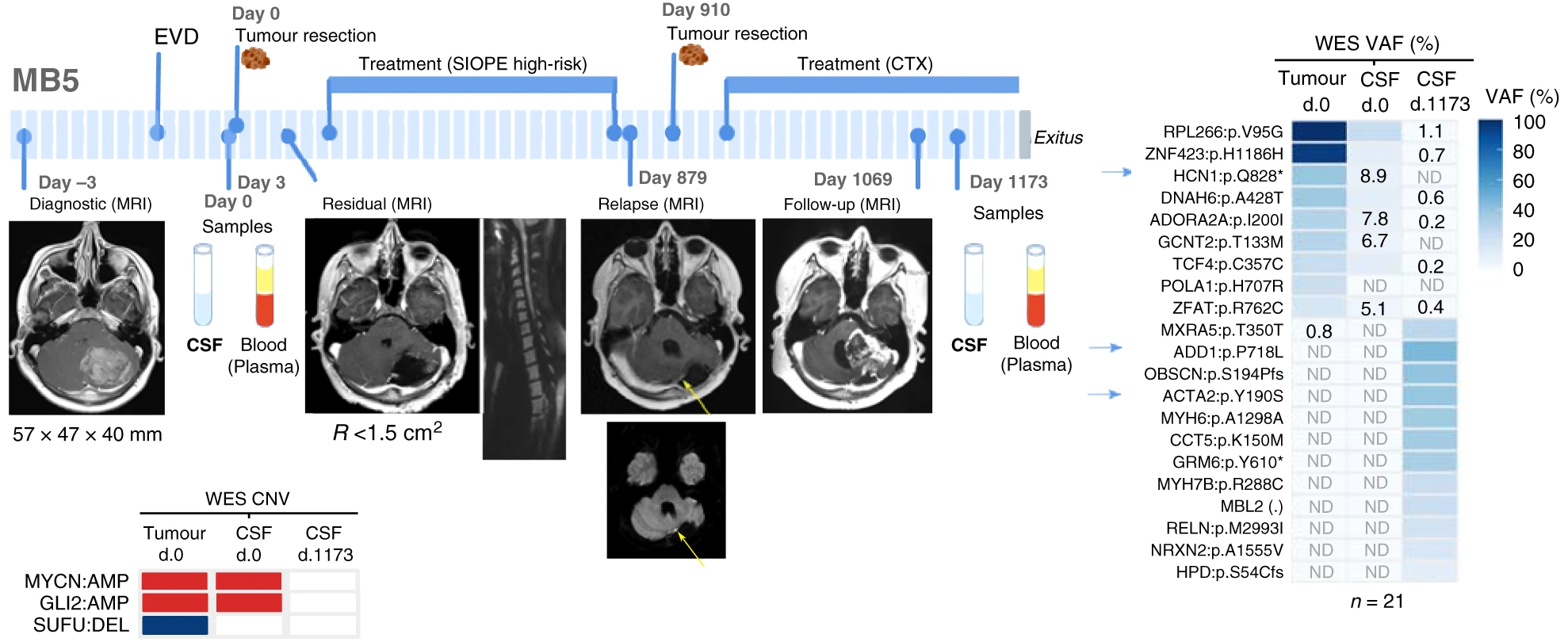
En pacientes pediátricos suele ser muy habitual la hidrocefalia, que requiere la extracción periódica de líquido cefalorraquídeo, lo que facilita las biopsias propuestas. Los meduloblastomas pueden tener pronósticos muy diferentes, pues algunos tumores son mucho más agresivos que otros; la biopsia propuesta permite caracterizar el pronóstico lo que facilita que el neurocirujano pueda extirpar más o menos cantidad del tumor en función de su agresividad. El ctDNA permite clasificar los tumores en función de la frecuencia de alelos variantes (VAF) asociadas a las mutaciones en el tumor. Las repercusiones traslacionales del nuevo trabajo son enormes, como descubrir casos en los que los tumores no son visibles en la imagen tomográfica, o mejorar el trabajo de los neurocirujanos, o las quimioterapia.
El artículo es Laura Escudero, Anna Llort, …, Joan Seoane, «Circulating tumour DNA from the cerebrospinal fluid allows the characterisation and monitoring of medulloblastoma,» Nature Communications 11: 5376 (27 Oct 2020), doi: https://doi.org/10.1038/s41467-020-19175-0.
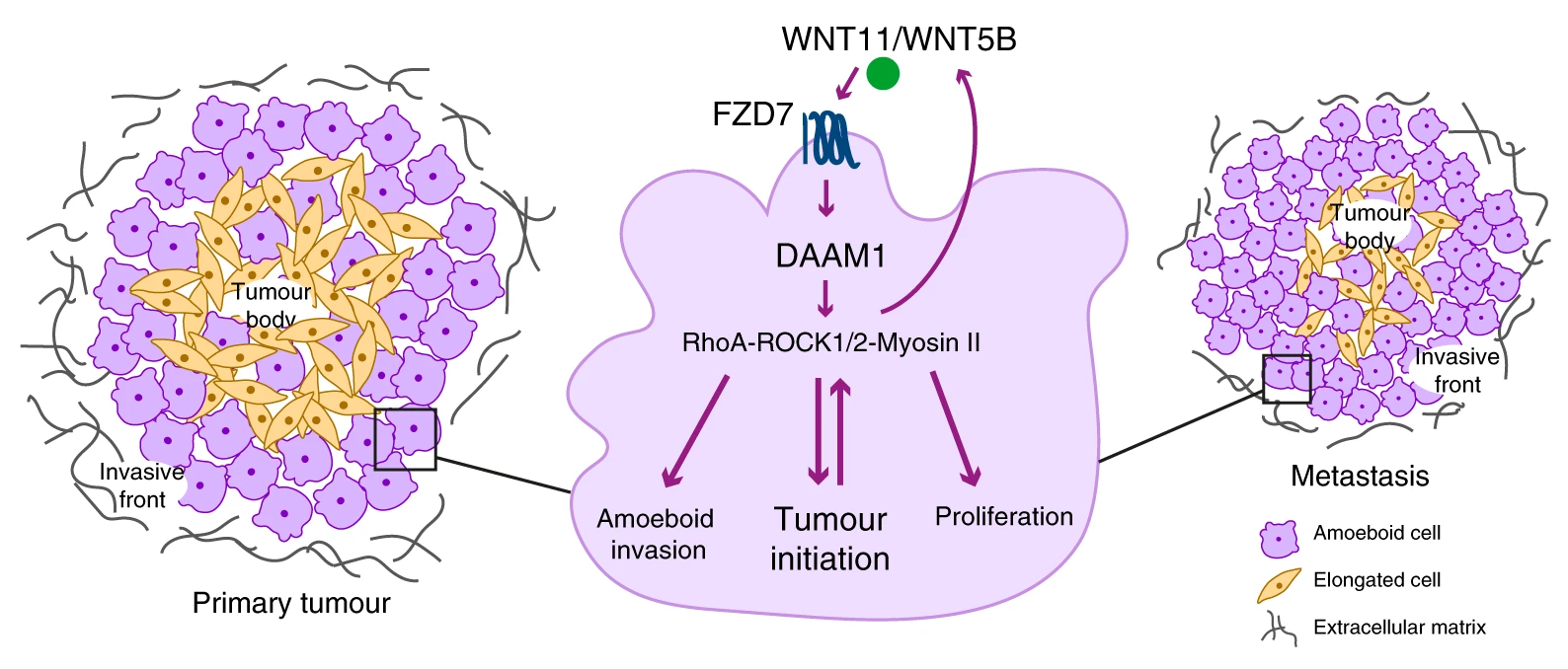
Pepe nos presenta un artículo de Victoria (Vicky) Sanz-Moreno (Barts Cancer Institute, Queen Mary University of London, Londres, Reino Unido) y sus colegas sobre el estudio ómico de los melanomas, que son tumores muy agresivos y forman metástasis en todas las partes del cuerpo. Se trata de un estudio que caracteriza el llamado frente invasivo del tumor; las células del borde del tumor son muy peligrosas porque son muy invasivas y además son inmunosupresoras; más aún, estas células del borde resisten a muchos tratamientos contra el melanoma. Los estudios ómicos permiten determinar los puntos débiles de estas células para el futuro desarrollo de terapias específicas.
Hay una ruta de señalización que involucra la citoquina ROCK que activa la miosina II (llamada Rho-ROCK1/2-Myosin II) y que está relacionada con la contractibilidad de las células del borde del tumor. Las células de la cresta neural son multipotentes y supermigratorias, siendo las células madre que dan origen a los melanocitos; por ello los melanocitos tienen una gran capacidad supermigratoria. En el nuevo artículo se desvelan el papel crucial de una ruta WNT11-FZD7-DAAM1 que activa a la Rho-ROCK1/2-Myosin II. Se ha identificado un nuevo biomarcador ALDH1A1 asociado a los casos más peligrosos, lo que permitirá desarrollar un futuro kit de diagnóstico. Además, se propone el uso de inhibidores de estas rutas tras la cirugía (que ya elimina la parte del borde de los tumores).
El artículo Irene Rodriguez-Hernandez, Oscar Maiques, …, Victoria Sanz-Moreno, «WNT11-FZD7-DAAM1 signalling supports tumour initiating abilities and melanoma amoeboid invasion,» Nature Communications 11: 5315 (20 Oct 2020), doi: https://doi.org/10.1038/s41467-020-18951-2.

En el apartado de bionoticias se incorpora Iker a la tertulia y empieza con los galardonados Premios Rei Jaume I de 2020. «Los galardonados han sido anunciados en un acto formal en el Palau de la Generalitat presidido por el jefe del Consell, Ximo Puig, y que ha contado con la presencia del presidente fundador, Santiago Grisolía, del presidente ejecutivo, Javier Quesada, además del vicepresidente de la Fundación Premios Rei Jaume I, Vicente Boluda. Los ganadores son Francisco José García Vidal, en la categoría de Investigación Básica, Diego Puga Pequeño, en Economía, Miguel Beato del Rosal, en Investigación Médica, Fernando Maestre Gil, en Protección del Medio Ambiente, Laura M. Lechuga Gómez, en Nuevas Tecnologías, y Verónica Pascual Boé, en el premio al Emprendedimiento».
Iker se centra en Miguel Beato del Rosal, premiado «por su trabajo pionero con el descubrimiento de ciertas proteínas que actúan de receptores de hormonas esteroides, incluido el receptor de glucocorticoides. Caracterizó el receptor de progesterona y encontró que los receptores esteroides se unen a porciones específicas de la secuencia de ADN. También encontró cómo los complejos remodeladores de cromatina modulan la estructura de los nucleosomas y la transcripción de genes, contribuyendo a explicar la expresión génica. Beato, fue fundador en 2000 y primer director del CRG (Centro de Regulación Genómica) de Barcelona, toda una «una fábrica de buenos investigadores». El modelo de funcionamiento y gestión del CRG fue importado de Estados Unidos y prima la excelencia, el fichaje de los mejores científicos jóvenes, que al llegar al centro cuentan con los medios tecnológicos más punteros para desarrollar sus proyectos de investigación».

Nos cuenta Belén que la FDA aprueba el primer tratamiento contra el Ébola. «La FDA aprobó el pasado 14 de octubre el uso de Inmazeb, un cóctel de anticuerpos diseñados en laboratorio, para el tratamiento de adultos y niños afectados por Ébola. Este tratamiento es producido por la farmacéutica Regeneron. El anuncio se da un año después de la aprobación de la primera vacuna contra el Ébola, la vacuna Ervebo de Merck. El Ébola es una de las enfermedades víricas más mortales: puede llegar a matar al 90% de los infectados y hasta ahora no se disponía de tratamientos efectivos, solo terapias de apoyo para evitar la deshidratación extrema».
«Inmazeb ha sido testeado junto a otros tres fármacos en un ensayo clínico realizado en Congo entre 2018 y 2019, durante el segundo brote más grande de esta enfermedad. Durante este, el 33,8% de los pacientes tratados murieron tras 28 días, frente a un 51% que falleció tras recibir otro tratamiento.
Inmazeb es concretamente es una mezcla de tres anticuerpos monoclonales diferentes. Uno se adhiere a la estructura del virion e implide que infecte las células, mientras que los dos restantes facilitan el reclutamiento de células del sistema inmune. Se aplica por vía intravenosa».
Iker recalca que hay que «recordar que este mismo año África fue declarada territorio libre de polio. En medio de esta pandemia, no todo son noticias malas con respecto a los virus.»

La siguiente bionoticia nos la presenta Iker, la publicación el pasado 19 de octubre del borrador borrador del proteoma humano. Este hito de la Organización del Proteoma Humano (HUPO) que se creó en el año 2001 y continúo el Proyecto Proteoma Humano (HPP) que se inició en septiembre de 2010. En este logro han participado unos 400 científicos de 25 países, lográndose descifrar el 90 % del proteoma humano, identificándose 17 874 proteínas procedentes de unos 19 773 genes codificantes (de proteínas) en el genoma humano. Este borrador contiene datos de muy alta calidad; no obstante, se aventura que conseguir el 10 % restante (las llamadas «proteínas faltantes», del inglés missing proteins) será tarea difícil. El proteoma humana abrirá puertas al descubrimiento de nuevas dianas para fármacos y a desvelar las bases moleculares de muchas enfermedades.
Esta bionoticia viene al hilo de un par de artículos sobre el proteoma: Subash Adhikari, Edouard C. Nice, …, Mark S. Baker, » A high-stringency blueprint of the human proteome,» Nature Communications 11: 5301 (16 Oct 2020), doi: https://doi.org/10.1038/s41467-020-19045-9, y Christopher M. Overall, «The HUPO High-Stringency Inventory of Humanity’s Shared Human Proteome Revealed,» Journal of Proteome Research (19 Oct 2020), doi: https://doi.org/10.1021/acs.jproteome.0c00794.

Entrevistamos a Juan Antonio Vizcaíno, que dirige el grupo de proteómica del Instituto Europeo de Bioinformática (EBI), perteneciente al Laboratorio Europeo de Biología Molecular (EMBL) en Cambridge, Reino Unido. Le pregunta Belén «¿cómo fueron los inicios del Proyecto Proteoma Humano?». Nos cuenta Juan Antonio que en España se trabajó en el cromosoma 16 y que es una colaboración internacional durante diez años en la que han intervenido muchos grupos. Pregunta Belén «¿cómo se organiza el proyecto y cuáles han sido los logros alcanzados?», a lo que responde Juan Antonio sobre las dificultades que conlleva un proyecto que maneja tantos datos, ya conocidos y nuevos, y que requieren un protocolo muy bien definido para unificar los formatos de todos esos datos. Las dos aproximaciones usadas son reusar datos ya existentes y generar nuevos datos de laboratorio.
Pregunta Iker «¿qué son exactamente las proteínas PE1 y qué son las proteínas faltantes (missing proteins)?» Nos responde Juan Antonio que hay proteínas que solo se expresan en ciertas células, con lo que son difíciles de estudiar. Y, además, hay proteínas cuyas concentraciones son muy, muy bajas, con lo que son muy difíciles de ver, y además las proteínas con mayor concentración velan a las de menor.
Pregunto por qué se dice que hay unas 100 000 proteínas pero solo unos 20 000 genes. Nos contesta que el objetivo del proyecto es mapear la forma canónica de la proteína por cada gen; pero muchos genes codifican muchas proteoformas (proteoforms). Tanto isoformas (resultado del splicing alternativo), que no se conocen para todos los genes, como otras muchas modificaciones adicionales (como las postranslacionales, proteínas fosforiladas, …). El proyecto Human Proteoform Project está empezando a dar sus primeros pasos.
Belén pregunta «¿cree que el proteoma ha quedado un poco fuera de los focos? Al fin y al cabo, la obtención del genoma humano fue un éxito celebrado por todo lo alto, mientras que este borrador del proteoma ha generado un ruido discreto. ¿Por qué no tiene el mismo impacto mediático e, incluso, entre la comunidad científica que la publicación del genoma humano?» Contesta Juan Antonio…
Pepe comenta «que el objetivo del proteoma es «traducir el código de la vida» (translating the code of life) lo que implica un salto en complejidad respecto al genoma humano». Comenta Juan Antonio que el genoma ha tenido más aplicabilidad a la sociedad en general que el proteoma; aunque este último también promete aplicaciones futuras.
Silvana pregunta «¿qué recursos computacionales y humanos son necesarios para manejar tan ingente cantidad de datos?» Juan Antonio contesta que se requieren grandes infraestructuras que solo están disponibles en centros de supercomputación. Y por supuesto se requiere el personal con los conocimientos suficientes para realizar el análisis y la integración de los datos. Lograr que ambas cosas, infraestructuras y personal, es todo un reto.
Finalmente, Iker pregunta «¿cómo serán los esfuerzos futuros para disminuir ese «gap» del 10 % faltante?» Nos comenta Juan Antonio que se están usando análisis de transcriptómica y los nuevos avances en la instrumentación de laboratorio; un punto clave en proteómica es la preparación de las muestras, para que los análisis sean repetibles; y también las propiedades fisicoquímicas de algunas proteínas producen grandes dificultades, u otras son muy pequeñas; la gran heterogeneidad de las proteínas supone enormes retos comparado con el genoma. Y muchas más cosas, un poco de todo y mucha paciencia. Este último 10 % va a llevar mucho tiempo, pero se logrará.

Silvana nos presenta un artículo publicado en Science sobre la relación entre la microbiota y la radioprotección (supervivencia a la radiación ionizante). El objetivo es estudiar en ratones cómo afecta la radioterapia oncológica sobre la composición microbiona gastrointestinal. Se ha comparado el microbioma de ratones que sobreviven a altas dosis de radiación con el resto (que no sobrevivieron); esta «élite superviviente» albergaba un microbioma intestinal diferenciado (enriquecido en bacterias Lachnospiraceae y Enterococcaceae, que parecen tener un papel radioprotector). Para destacar la relevancia clínica de este estudio en humanos se analizaron un pequeño grupo de pacientes con leucemia expuestos a radiación. Se observó que una elevada abundancia de Lachnospiraceae y Enterococcaceae en su microbiota está asociada a menos efectos adversos.
Además, en ratones, se observó que el propionato presenta una actividad radioprotectora (atenúa el daño del ADN y la libera especies reactivas con el oxígeno en los tejidos hematopoyéticos y gastrointestinales). También se observó que dos metabolitos de la vía del triptófano, 1H-indol-3-carboxaldehído (I3A) y ácido quinurénico (KYNA), también proporcionan radioprotección a largo plazo en los ratones. Así se concluye que no solo la microbiota intestinal es crucial en la defensa contra la radiación, sino que ciertos metabolitos relacionados con el propionato y el triptófano podrían ser usadas como terapia radioprotectora (reduciendo síntomas secundarios asociados a la radioterapia).
Silvana lo cuenta en el podcast mucho mejor que yo en este breve resumen. El artículo es Hao Guo, Wei-Chun Chou, …, Jenny P. Y. Ting, «Multi-omics analyses of radiation survivors identify radioprotective microbes and metabolites,» Science 370: eaay9097 (30 Oct 2020), doi: https://doi.org/10.1126/science.aay9097. También recomiendo el reciente Melissa C.Kordahi, BenoitChassaing, «The Intestinal Microbiota: Our Best Frenemy in Radiation-Induced Damages?» Cell Host & Microbe 29: 7-9 (13 Jan 2021), doi: https://doi.org/10.1016/j.chom.2020.12.013.
Lo dicho, ¡qué disfrutes del podcast!

