Para los que jugamos a los dardos, un «hat-trick» es cuando un jugador logra tres dianas. Supongo que J. Corbella utiliza su significado futbolístico, un jugador que marca tres goles en un solo partido. En cualquier caso Luis Serrano ha logrado un «´Hat-trick´ científico,» como muy bien nos relata J. Corbella en La Vanguardia, tres, sí, tres artículos en un mismo número de Science [visto en Menéame], que presentan el transcriptoma, metaboloma y proteoma de la bacteria Mycoplasma pneumoniae. Un hecho insólito por partida triple al que yo quise dedicarle una entrada, ayer, pero 24 horas sin Internet, gracias a la «amabilidad» de Orange, no me lo permitieron. Mi idea era contar este gran logro científico desde mi punto de vista, obviamente sesgado por mi formación e inquietudes. Aunque algunos me comparen con Sokal, el que quiera que me lea y el que no, que acuda a otras fuentes.
Por supuesto, en La Vanguardia también lo explican, copiando la noticia de la agencia Europa Press, «Desvelan la complejidad de la vida en la bacteria más pequeña analizada. La ‘Mycoplasma pneumoniae’ podría ayudar a los científicos a determinar la mínima maquinaria celular necesaria para la vida,» 26/11/2009 [también meneada]. A mí me gusta más la versión de El País, algo más europeista, «La vida es más compleja de lo que se esperaba. Investigadores europeos definen los requisitos de funcionamiento de una célula autosuficiente,» 26/11/2009. Faltaría más, mi mujer prefiere la versión de El Mundo, Rosa M. Tristán, «Estudio Español. En busca de una ‘píldora’ con vida. Revelan la complejidad de una célula mínima que podría servir de medicamento,» 26/11/2009. ¿Cuál prefieres tú? Todos los medios se han hecho eco de esta gran noticia… seguro que tú prefieres no seguir leyendo lo que yo pueda contar, en mi ignorancia, al respecto.
Lo que sigue es una traducción libre resumen de la Perspective de Howard Ochman y Rahul Raghavan, «Excavating the Functional Landscape of Bacterial Cells,» Science 326: 1200-1201, 27 November 2009. Obviamente se hacen eco de los tres artículos técnicos de los que uno de los investigadores principales es Luis Serrano: Marc Güell et al., Anne-Claude Gavin, Peer Bork, Luis Serrano, «Transcriptome Complexity in a Genome-Reduced Bacterium,» Science 326: 1268-1271, 27 November 2009; Eva Yus et al., Anne-Claude Gavin, Peer Bork, Luis Serrano, «Impact of Genome Reduction on Bacterial Metabolism and Its Regulation,» Science 326: 1263-1268, 27 November 2009; y Sebastian Kühner et al., Luis Serrano, Peer Bork, Anne-Claude Gavin, «Proteome Organization in a Genome-Reduced Bacterium,» Science 326: 1235-1240, 27 November 2009.
Mycoplasma pneumoniae es una bacteria procariota (sin núcleo) responsable de un 40% de las neumonías, infecciones respiratorias agudas, en niños. Se estima que en el mundo mueren 2 millones de niños al año por esta causa. Para los investigadores en genómica esta bacteria es una de las células más estudiadas ya que su genoma es el más pequeño conocido de una bacteria capaz de autorreplicarse sin ayuda y vivir fuera de un huésped. Ello permite que pueda ser cultivada en laboratorio (in vitro) y que se pueda estudiar la respuesta de su metabolismo ante cambios controlados en su medio de cultivo. Su genoma, de sólo 816.394 nucleóticos (bases), tiene 689 genes codificadores de proteínas (que estén anotados) y sólo 44 moléculas de ARN no codificadoras.
El metabolismo de una bacteria como M. pneumonie se suele comparar con el de la bacteria modelo Escherichia coli. Si un gen particular o una vía metabólica está ausente en el genoma de la bacteria, se suele asumir que esta bacteria no puede desarrollar dicha función metabólica y por tanto que dicha función no es requisito indespensable para la supervivencia de un organismo. Esta asociación uno a uno entre gen y función es más fe que ciencia, como han demostrado los tres artículos de Luis Serrano y colaboradores en Science. La organización de su red de proteínas (proteoma) y de su red de control de la transcripción (transcriptoma) es mucho más sutil y compleja de lo que se pensaba. Pocos podían pensar que se pareciera tanto a los mecanismos propios de las células eucariotas (con núcleo). Un genoma tan simple y a la vez tan capaz de desarrollar un metabolismo tan complejo. Esta es la gran sorpresa que se ha descubierto con el gran trabajo desarrollado por Serrano y sus colaboradores europeos.
El transcriptoma de este Mycoplasma es analizado en el artículo de Marc Güell et al. quienes han descubierto un transcriptoma muy complejo, similar al de las células eucariotas. Han encontrado 117 nuevos genes de ARN no codificantes, identificado 341 operones, 139 de los cuales son policistrónicos (contienen más de un gen) y, para su sorpresa, observado que estos operones se dividen en 447 unidades de transcripción más pequeñas. El resultado es una maquinaria de control de la transcripción del genoma mucho más complicada de lo que se esperaba, ya que las bacterias con genomas pequeños se pensaba que tenían muy pocos factores de transcripción.

El metaboloma de M. pneumoniae es analizado en el artículo de Eva Yus et al. quienes han reconstruido la red metabólica de esta bacteria utilizando un «curado» manual basado en toda la información bioquímica, estructural y computacional disponible. Dicha red les ha permitido determinar el medio de cultivo mínimo que permite mantener con vida y cultivar a esta bacteria. La red metabólica descubierta contiene 189 reacciones químicas catalizadas por 129 enzimas que permiten sobrevivir a la bacteria en un medio mínimo que contenga sólo 19 nutrientes esenciales. Comparar las rutas metabólicas de esta bacteria con otras, como las de E. coli, muestra que tiene muchas menos rutas o redundancias, sin embargo, presenta muchas más enzimas que realizan más de una función. Esta multiplicidad funcional está regulada por el complejo transcriptoma encontrado por Marc Güell et al. Sorprende que, aunque siendo mucho más simple, las características generales del metabolismo encontrado son similares a las de otras bacterias, así como su capacidad de adaptarse y responder rápidamente ante cambios en la concentración de metabolitos en su medio.
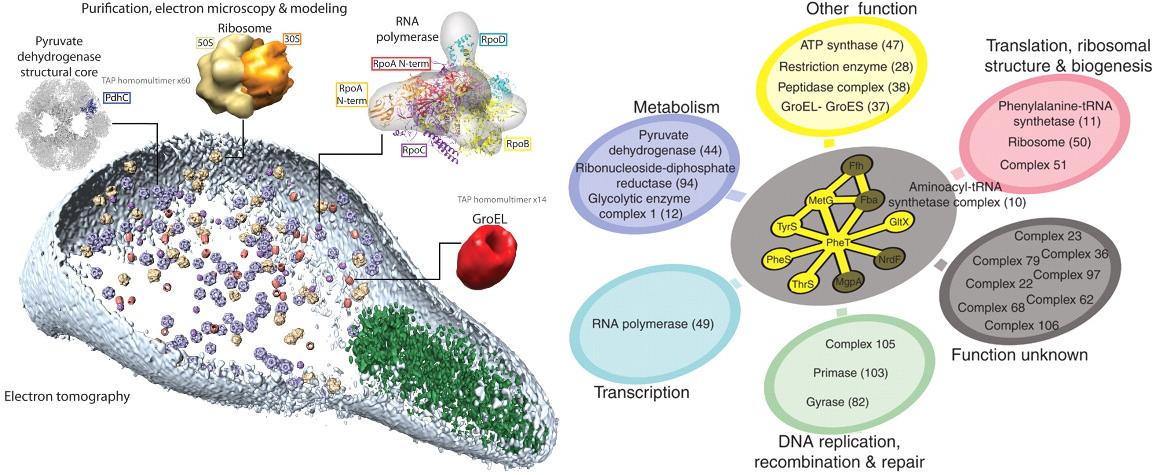
El proteoma de M. pneumoniae es analizado por Sebastian Kühner et al. y también muestra una complejidad mayor de la esperada. Como ocurre con las células eucariotas, más del 90% de las proteínas solubles de M. pneumoniae son componentes de complejos protéicos, en concreto, 62 homomultiméricos y 116 heteromultiméricos (la mayoría desconocidos hasta ahora). Los investigadores también han estudiado la estructura tridimensional de 484 proteínas, han obtenido imágenes de microscopía electrónica (como la de abajo) y tomogramas celulares que permiten observar la organización y localización de las proteínas dentro de la bacteria. Es sorprendente que la red de interacciones entre proteínas se correlaciona pobremente con la organización del genoma y del transcriptoma. Hay genes adyacentes o que se expresan simultáneamente cuyas proteínas asociadas no interactúan entre sí. Inferir toda esta complejidad sólo a partir del genoma parece completamente imposible, más aún teniendo en cuenta el gran número de proteínas multifuncionales encontradas.
¿Cómo la evolución ha sido capaz de lograr un organismo tan simple regulado de una forma tan compleja? La opinión más obvia es que el genoma de esta bacteria ha evolucionado por reducción del número de genes. La acumulación de mutaciones perjudiciales en el genoma ha llevado a que los genes dañados hayan sido eliminados reduciendo así el tamaño del genoma. Conforme los genes se han ido perdiendo, su papel ha sido tomado por los genes restantes, quizás los que cooperaban con ellos en realizar las mismas funciones. Este proceso de sustitución ha conducido a una complicada red de regulación y al desarrollo de nuevas rutas metabólicas. En este sentido, esta bacteria considerada antes como ejemplo ideal de bacteria «simple» en realidad no lo es. Algo parecido puede ocurrir con las bacterias con los genomas más pequeños que existen, como la bacteria simbiótica Hodgkinia cicadicola, con sólo 144 kb (kilobases o miles de nucleótidos), que codifica sólo 15 ARN de transferencia (ARNt) para lograr especificar los 20 aminoácidos que requiere para sintetizar proteínas. Con toda seguridad muchos de dichos ARNt cumplirán funciones múltiples como las observada en el «hat-trick» de Luis Serrano y colaboradores en Science.



Comparar los muy instructivos textos de Francis con la broma de Sokal en «Social Text» es una de las barbaridades mayores que he leído últimamente.
Dice Confucio: ¿Acaso no es propio del hombre superior no enojarse al no ser reconocido? (Analectas 1,1). Sigue el consejo del venerable sabio y no te enojes, Francis.
Pues yo me quedo con el tuyo, Francis.
Una notilla sólo: la neumonía causada por este bicho es lo que se llama una neumonía atípica, ya que no presenta los síntomas habituales.
Una extrañeza: hasta donde yo sé los Mycoplasmas son parásitos obligados, es decir, no pueden vivir fuera del huésped.
Un cordial saludo.
Gracias, César. Tienes razón por tu extrañeza. Sin embargo, como son autorreproductores, no necesitan de la maquinaria de replicación del ADN del huésped, se pueden cultivar en laboratorio (in vitro). Que yo sepa, esto se sabe desde 1956, cuando se contaminaron unos cultivos con este mycoplasma y se observó su reproducción in vitro (http://dx.doi.org/10.1126/science.124.3232.1147). Hoy en día, se sabe cultivar in vitro prácticamente todos los mycoplasmas.
Es un trabajo espectacular. Lo que no entiendo es cómo aún quieren recortar el presupuesto en investigación. Impresionante.