En el punto triple del agua (a 0,01 °C de temperatura y 612 pascales de presión) coexisten en equilibro sus tres estados sólido, líquido y gaseoso. El dióxido de vanadio es un sólido que presenta un punto triple a 65 °C en el que coexisten tres fases sólidas, dos aislantes (con estructuras cristalinas monoclínicas, M1 y M2) y una conductora (con estructura tetragonal tipo rutilo, R). Gracias a un dispositivo micromecánico se ha medido con alta precisión el diagrama de fase temperatura versus esfuerzo en tracción de una nanobarra de dióxido de vanadio (VO2). Películas delgadas de óxido de vanadio se utilizan mucho en la industria electrónica y en óptica física como «material inteligente» (porque sus propiedades varían mucho con la temperatura y el voltaje aplicado). La más interesante de las tres fases es M2 ya que no hay ninguna teoría microscópica que explique su estabilidad; el nuevo diagrama de fase guiará los cálculos de la estructura electrónica mediante ordenador, lo que quizás ayude a aclarar este asunto. Existen puntos triples sólidos en la manganita y en niquelatos de tierras raras, aunque aplicar el nuevo método de medida no será fácil pues se requieren nanobarras de muy alta calidad. Nos lo cuenta Douglas Natelson, «Condensed-matter physics: A solid triple point,» Nature 500: 408–409, 22 Aug 2013, que se hace eco del artículo técnico de Jae Hyung Park et al., «Measurement of a solid-state triple point at the metal–insulator transition in VO2,» Nature 500: 431–434, 22 Aug 2013.
En las tres fases del dióxido de vanadio hay dos conjuntos de cadenas paralelas de átomos de vanadio (en negro en la figura), cada uno rodeado de seis átomos de oxígeno (no mostrados en la figura) que forman un octaedro distorsionado. En la fase R (de tipo rutilo), a alta temperatura, todas las cadenas son rectas y periódicas, mientras que en la fase M1 (monoclínica) todos los átomos de vanadio forman dímeros. Hay otras dos fases aislantes; la fase M2 (monoclínica) en la que sólo una de las cadenas de átomos de vanadio forma dímeros y la fase T (triclínica) intermedia entre M1 y M2. Las dos fases monoclínicas tienen propiedades aislantes similares. La mayor diferencia en la celda unidad entre las tres fases R, M1 y M2 es la distancia interatómica en el eje longitudinal de las cadenas (eje c de la estructura tipo rutilo), en concreto c(R) = 5,700 Å, c(M1) = 5,755 Å y c(M2) = 5,797 Å.
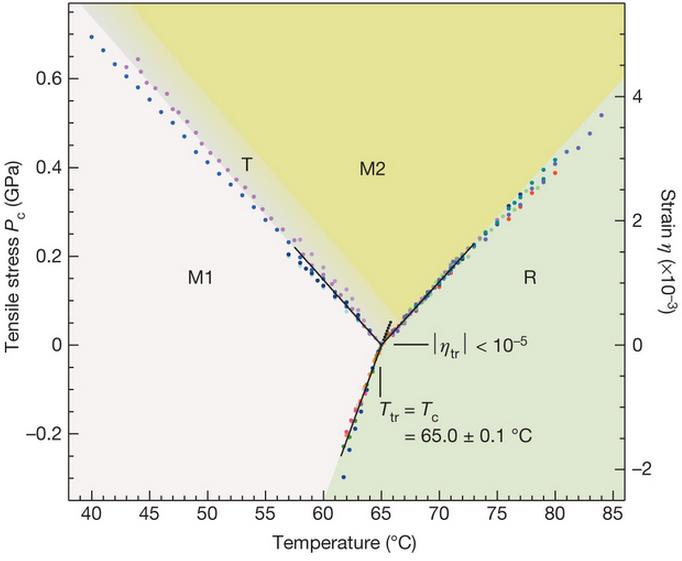
Para estudiar el punto triple del dióxido de vanadio se comprime una nanobarra en la dirección del eje de las cadenas de átomos de vanadio mientras se cambia la temperatura. El punto triple ocurre a una temperatura de 65,0 ± 0,1 °C y se observa gracias a una discontinuidad en el diagrama plano que relaciona la longitud de la nanobarra y la temperatura.
En mi opinión, lo más interesante de este trabajo es que nos recuerda que aún muchas propiedades electrónicas de los materiales sencillos que no sabemos calcular de forma teórica. Se espera que el intento de reproducir mediante simulaciones por ordenador el diagrama de punto triple obtenido en los experimentos permitirá desarrollar una teoría microscópica que explique las transiciones M1-M2 y R-M2, lo que a su vez ayudará a diseñar mejores películas de «materiales inteligentes» para aplicaciones prácticas.





Personalmente hablando Los Puntos Triples de Estado fueron el tema peor explicado de toda mi formación universitaria. No entendí nada por que de la forma en que recibí la materia no había forma de entender algo. Las únicas personas que comprendieron algo sobre Los Puntos Triples fueron los fuera de serie de mi promoción que solían disponer tiempo para consultar bibliográficas. Esas mentes privilegiadas que disponían de tiempo para prepararse los temas con antelación al profesor se miraban ahítos entre si durante esas clases al oír al profesor. Fue bochornoso.