
Ya puedes disfrutar del episodio 5 del podcast Biosíntesis [Medium, iVoox, iTunes, Google podcasts, Spotify, TuneIn, Radio Public, PlayerFM]. Cada quince días (aunque en esta ocasión nos hemos retrasado un poco) presentamos artículos científicos sobre bioquímica y biología molecular relevantes en biomedicina. Fue grabado el lunes 06 de mayo de 2019 en el estudio de radio de la Facultad de Ciencias de la Comunicación de la Universidad de Málaga (UMA). Bajo la batuta de José (Pepe) Lozano @leviaingenia (Dep. Biología Molecular y Bioquímica, UMA), participamos Silvana Tapia @SilvanaTapia3 (Dep. Microbiología , UMA), y un servidor, Francisco R. (Francis) Villatoro, @emulenews (Dep. Lenguajes y Ciencias de la Computación, UMA).
Además de nosotros, nos acompañaron en el programa dos jóvenes estudiantes, Belén Delgado Martín (Grado de Bioquímica, UMA) e Íker Puerto San Román, @SrMitocondrio (Grado de Bioquímica, UMA), autor del blog La Mitocondria. Finalmente, en nuestra sección de reseñas hemos entrevistado a los traductores al español de «Mi vida en la ciencia» la biofonía de Sydney Brenner, Juli Peretó y Emilia Matallana, así como a un amplio plantel de investigadores que han conocido al genial Brenner. Más información sobre el contenido del podcast en “Episodio BS#5,” Medium, 11 May 2019.
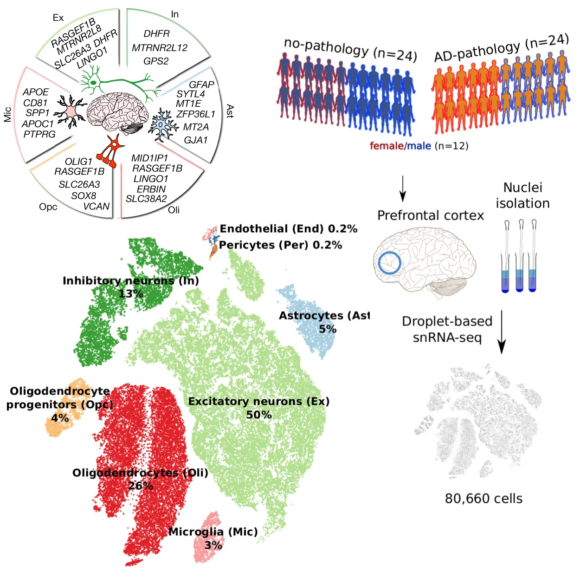
Empieza hablando un servidor sobre dos artículos relacionados con el Alzheimer. Hansruedi Mathys et al publican en Nature el 01 de mayo de 2019 el transcriptoma asociado a la enfermedad de Alzheimer. Se han identificado los genes expresados vía los ARN transcritos en 80 660 células de la corteza prefrontal de 48 individuos con diversos grados de patología. Los cambios más significativos se encuentran en los genes relacionados con la regeneración de los axones y la mielinización. El hallazgo más sorprendente han sido las diferencias entre sexos (pacientes masculinos y femeninos); no está claro por qué existe esta discrepancia. Un primer paso de gran relevancia para desvelar bases moleculares y celulares de esta enfermedad neurodegenerativa. El artículo es Hansruedi Mathys, Jose Davila-Velderrain, …, Li-Huei Tsai, “Single-cell transcriptomic analysis of Alzheimer’s disease,” Nature (01 May 2019), doi: 10.1038/s41586-019-1195-2.

Manolis Kellis y Li-Huei Tsai, director del Instituto Picower para el aprendizaje y la memoria del MIT, son los autores principales del estudio, habiendo contribuido por igual Hansruedi Mathys y Jose Davila-Velderrain, postdocs en el MIT. Su estudio de muestras del encéfalo de 48 individuos, 24 con Alzheimer y 24 sin signos de esta neuropatología. Se estudiaron las células más abundantes, neuronas excitadoras e inhibidoras, y células menos abundantes, como oligodendrocitos, astrocitos y microglia. Los cambios más significativos se observan en la expresión de genes relacionados con la regeneración de los axones y la mielinización; recuerda que la mielina rodea los axones y ayuda en la transmisión del impulso nervioso, siendo los oligodendrocitos los que producen la mielina. La mayoría de los cambios observados en la expresión génica ocurren en una fase temprana del desarrollo de la enfermedad. También se han observado correlaciones en los patrones de expresión génica y los síntomas asociados a la gravedad del Alzheimer, como el nivel de placas betaamiloides y ovillos neurofibrilares de proteína tau. Así se han podido identificar cierta modularidad en la expresión génica, aunque no se conoce la función de cada uno de los «módulos».

En mi opinión, lo más curioso es que hay dimorfismo sexual en la expresión génica, es decir, diferencias entre hombres y mujeres. Un hallazgo sorprendente incluso para los propios investigadores. Las neuronas excitadoras y otras células de los pacientes masculinos muestran cambios en la expresión génica menos pronunciados en la enfermedad de Alzheimer que las células de los pacientes femeninos, a pesar de que los síntomas en ambos casos son muy similares. Se ignora la causa de esta discrepancia. Este dimorfismo sexual está más marcado en los oligodendrocitos, que producen mielina; usando imágenes de resonancia magnética de 500 pacientes adicionales se desveló que las mujeres con graves déficits de memoria tienen más daño en la sustancia blanca que los hombres con síntomas simlares.

Por otro lado comento el artículo que Peter T. Nelson et al publican en Brain el 30 de abril de 2019 la identificación de un nuevo tipo de demencia, llamada LATE, que aparece en más del 20% de los cerebros de las personas de más de 80 años, y que hasta ahora podría haber sido confundido con el alzhéimer. LATE es el acrónimo de «encelopatía TDP-43 límbico-predominante relacionada con la edad». Quizás, muchos de los ensayos clínicos de tratamientos contra el alzhéimer fracasan porque están incluyendo a pacientes con LATE que deberían excluirse. En el nuevo tipo de demencia está implicada la proteína TDP-43, como la esclerosis lateral amiotrófica, en lugar de las proteínas beta amiloide y tau. El artículo es Peter T Nelson, Dennis W Dickson, …, Julie A Schneider, “Limbic-predominant age-related TDP-43 encephalopathy (LATE): consensus working group report,” Brain 2019: awz099 (30 Apr 2019), doi: 10.1093/brain/awz099.

Los autores reivindican la patología LATE y afirman que la padecen una cuarta parte de las personas de 85 años o más edad. Sus síntomas son similares al Alzheimer, en cuanto a problemas de memoria y demencia, pero su causa parece ser muy diferente. De hecho, en lugar de las placas betaamiloides y ovillos de proteína tau, LATE se caracteriza por una acumulación de la proteína TDP-43. Hoy en día no se conocen pruebas clínicas que identifiquen a LATE en una persona viva; el artículo solo presenta su diagnóstico postmorten.
Los investigadores reivindican esta patología para que se financie investigación básica que permita desarrollar herramientas de diagnóstico in vivo. Comento este artículo porque está relacionado con el Alzheimer. Los medicamentos para tratar el Alzheimer en estado muy avanzado se basan atacar las vías moleculares asociadas a la producción de placas betaamilodes. Estos medicamentos han fallado y muchas grandes farmacéuticas han abandonado su investigación en esta línea. Quizás dicho fallo es debido a que gran parte de los pacientes de avanzada edad que se supone que tenían Alzheimer en realidad tenían LATE; en dicho caso, se habría introducido un sesgo sistemático en la selección de pacientes que enmascara los posibles resultados positivos de los medicamentos. Quizás hay que reevaluar todos estos ensayos clínicos. Sin lugar a dudas, toda una revolución indirecta en el estado actual de los tratamientos contra el Alzheimer.
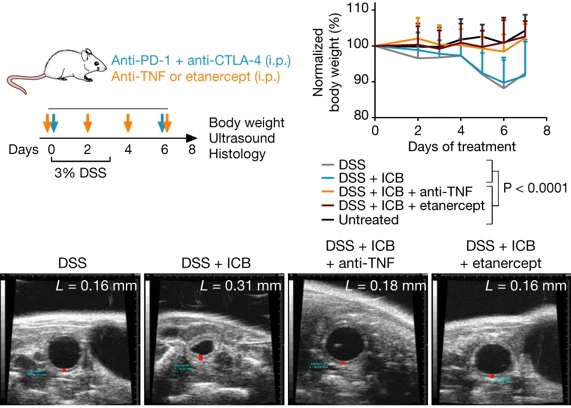
Pepe nos habla de un artículo de su amiga Elisabeth Perez-Ruiz et al., Nature (01 Apr 2019), que presenta un nuevo tratamiento del cáncer más eficaz y menos tóxico. En ratones, al bloquear la proteína llamada factor de necrosis tumoral (en inglés TNF) durante un potente tratamiento de inmunoterapia contra el cáncer (terapia que combina dos medicamentos: el anti-PD-1 y anti-CTLA-4), se consigue mejorar su eficacia y reducir la toxicidad. El siguiente paso será trasladar esta investigación a la clínica. Te recomiendo la estupenda entrevista que Pepe le realiza a Elisabeth sobre su trabajo; solo quiero destacar que su primer artículo ha sido un Nature y todo gracias a un póster en una conferencia científica, que gustó a una editora de Nature que estaba por allí buscando temas interesantes. Así que, recuerda, los pósters en los congresos son mucho más relevantes de lo que puede parecer El artículo es Elisabeth Perez-Ruiz, Luna Minute, …, Ignacio Melero, “Prophylactic TNF blockade uncouples efficacy and toxicity in dual CTLA-4 and PD-1 immunotherapy,” Nature (01 May 2019), doi: 10.1038/s41586-019-1162-y.

Tras las bionoticias es el turno de Silvana que nos presenta el artículo de Thanabalasuriar et al. publicado en Cell Host & Microbe el 10 de abril de 2019. Se caracteriza la interacción entre los neutrófilos y las biopelículas de Pseudomonas en la córnea. En la base de la biopelícula, en los neutrófilos se expresa el sistema de secreción tipo 3 (T3SS), lo que lleva a una deposición y expansión de trampas extracelulares de neutrófilos (NET). La formación de las NET impide la diseminación de bacterias en el cerebro, pero promueve la resistencia a los antibióticos. El bloqueo del exopolisacárido Psl y de T3SS permite que los neutrófilos rompan la biopelícula. Ajitha Thanabalasuriar, Brittney Noelle Vivian Scott, …, Paul Kubes, “Neutrophil Extracellular Traps Confine Pseudomonas aeruginosa Ocular Biofilms and Restrict Brain Invasion,” Cell Host & Microbe 2: 1-11 (10 Apr 2019), doi: 10.1016/j.chom.2019.02.007.
En la sección de bionoticias tenemos a Belén Delgado y a Íker Puerto. Empieza Íker con la noticia «Muere un bebé participante en los ensayos de un revolucionario fármaco de Novartis», CincoDías, 23 abr 2019, un ensayo clínico de la farmacéutica Novartis contra la Atrofia Muscular Espinal (AME), una enfermedad neuromuscular causada por una mutación en el gen SMN1 (survival motor neuron 1). La empresa AveXis, propiedad de Novartis, está desarrollando Zolgensma, una terapia génica basada en un virus adenoasociado que porta una copia funcional del gen SMN1 y los lleva a las neuronas motoras. Hasta ahora, los estudios clínicos habían dado resultados muy prometedores. Pero ahora el progreso de este tratamiento se puede ver atascado por el fallecimiento de este niño de 6 meses tratado durante uno de los ensayos de la fase III de los estudios clínicos.

Nos comenta Belén la noticia de Rejji Kuruvilla, «Why brown fat has a lot of nerve,» Nature 569: 196-197 (01 May 2019), doi: 10.1038/d41586-019-01278-4. El gran aumento de la obesidad en la población mundial ha dado lugar a un incremento de la incidencia de diabetes y enfermedades cardiovasculares. El exceso de calorías en los mamíferos se acumula en forma de triglicéridos en el tejido adiposo blanco (grasa blanca), mientras que en el tejido adiposo marrón o grasa parda, se queman grasas y glucosa para producir calor en un proceso llamado termogénesis. La activación de este proceso es una potencial estrategia para el tratamiento de la obesidad, por lo que hay un gran interés por conocer el desarrollo y la fisiología de este tejido. El artículo Xing Zeng, Mengchen Ye, …, Bruce M. Spiegelman, «Innervation of thermogenic adipose tissue via a calsyntenin 3β–S100b axis,» Nature 569: 229-235 (01 May 2019), doi: 10.1038/s41586-019-1156-9, describe la función de la proteína calsintenina 3β, presente en las células de la grasa parda, como un regulador esencial de la inervación de la grasa parda y de la termogénesis mediante el control de la secreción de un factor de crecimiento, la proteína S100b.
Un regulador esencial de la termogénesis es el sistema nervioso simpático, que inerva a la grasa parda mucho más que a la grasa blanca y produce la liberación de noradrenalina, que desencadena la producción de calor en las mitocondrias. Zeng y col se propusieron investigar el proceso que controla la inervación de la grasa parda. Así, analizando los transcritos de RNA producidos en los adipocitos pardos, identificaron un gen no caracterizado previamente, el gen Clstn3b, que se expresa mucho y de forma muy selectiva en estas células. Además, la expresión puede inducirse en la grasa beige, que son adipocitos blancos que pueden convertirse en termogénicos ante algún estímulo, como el frío. Cuando los investigadores hicieron ratones KO para Clstn3b, los animales mostraban rápidamente hipotermia al ser sometidos al frío y eran más obesos que los wildtype. Por el contrario, los ratones que sobreexpresaban el gen tenían un menor peso corporal, mostraban más tolerancia al frío y eran resistentes a la obesidad inducida por la dieta. Todo esto indica que Clstn3b es necesario y suficiente para el proceso de termogénesis.
¿Cómo controla la calsintenina 3β la termogénesis? Los investigadores comprobaron que el sistema noradrenérgico (hemos dicho que es el que desencadena la termogénesis) estaba funcionando correctamente en los animales, pero la inervación de la grasa parda sí se había visto afectada ante los cambios en la expresión de Clstn3b, con una disminución de la inervación en los ratones KO y un aumento en los que lo sobreexpresan. La calsintenina 3β se encuentra en la membrana del retículo endoplasmático, un orgánulo en el que se sintetizan y secretan proteínas de membrana. La proteína que se regula negativamente en ausencia de calsintenina 3β es S100b, un factor de crecimiento que se expresa mucho en astrocitos. La calsintenina 3β interacciona físicamente con S100b y actúa como una chaperona que dirige y permite la secreción de la S100b formada desde el ER. Los ratones con deficiencia de S100b presentan una menor inervación que los wt, mientras que la expresión de S100b en los ratones KO para Clstn3b es suficiente para corregir el déficit de inervación y termogénesis. Este estudio puede ser la base para el desarrollo de estrategias terapéuticas que aumenten la inervación simpática de la grasa parda y potencien la termogénesis para combatir la obesidad y otros desórdenes metabólicos relacionados.

Finalmente, reseñamos el libro “Historia del cerebro” de José Ramón Alonso [LCMF, 11 mar 2019]. Te recomiendo la estupenda entrevista al autor, que nos demuestra toda su pasión por la neurociencia y por la divulgación. Merece la pena leer este libro.
Y sin más, ¡qué disfrutes del podcast tanto como nosotros al hacerlo!

