
Te recomiendo escuchar el podcast del episodio T02E34, «¿Y si la solución a la pandemia estuviera en tus genes?», 21 may 2020 [09:19 min], del programa de radio “Ciencia para todos”, en el que participo junto a Enrique Viguera (Universidad de Málaga), coordinador de Encuentros con la Ciencia. Esta sección semanal del programa “Hoy por Hoy Málaga” presentado por Isabel Ladrón de Guevara, se emite todos los jueves en la Cadena SER Málaga (102.4 FM) entre las 13:00 y 14:00 horas (no tiene hora fija de emisión en directo, pero suele ser entre las 13:05 y las 13:15). En este programa también ha intervenido Lola Calvillo e Ignacio San Martín. Todos hemos intervenido desde nuestras propias casas vía teléfono.
«El coronavirus se ha cebado con las personas más vulnerables, de edad avanzada o con patologías previas, pero también ha afectado a cierto número de jóvenes sanos. ¿Se sabe por qué ellos también son vulnerables al coronavirus? Se ha publicado que cuatro de cada diez personas pueden tener inmunidad previa frente al coronavirus, generada por exposición a otros patógenos, lo que podría explicar que haya tantos casos asintomáticos, ¿qué se sabe sobre este tema? No sabemos por qué algunos pacientes jóvenes y saludables enferman con síntomas severos y drásticas consecuencias. Tampoco sabemos por qué hay una mayor proporción de fallecimientos en hombres que en mujeres. Ni siquiera por qué algunas personas cursan la enfermedad de forma asintomática. Por ahora solo se trata de una hipótesis. Muchos especialistas en genética están tratando de identificar los cambios genéticos en las personas más susceptibles, se podría aconsejar a estas personas que adoptaran medidas más severas de prevención».
Más información divulgativa en Antonio Martínez Ron, «¿Haber pasado varios catarros te protege contra el coronavirus?» Next, Voz Pópuli, 19 may 2020; Enrique Viguera Mínguez, «¿Que seamos más o menos vulnerables al SARS-CoV-2 depende de nuestros genes?» The Conversation, 18 may 2020.
Los artículos citados son Alba Grifoni, Daniela Weiskopf, …, Alessandro Sette, «Targets of T cell responses to SARS-CoV-2 coronavirus in humans with COVID-19 disease and unexposed individuals,» Cell (14 May 2020), doi: https://doi.org/10.1016/j.cell.2020.05.015; Julian Braun, Lucie Loyal, …, Andreas Thiel, «Presence of SARS-CoV-2 reactive T cells in COVID-19 patients and healthy donors,» medRxiv preprint (22 Apr 2020), doi: https://doi.org/10.1101/2020.04.17.20061440. He extraído dos figuras del artículo de Sayoni Das, Krystyna Taylor, …, Steve Gardner, «Identification and Analysis of Shared Risk Factors in Sepsis and High Mortality Risk COVID-19 Patients,» medRxiv preprint (09 May 2020), doi: https://doi.org/10.1101/2020.05.05.20091918.
Escucha «¿Y si la solución a la pandemia estuviera en tus genes?» en Play SER.

ISABEL: Los malagueños ya estamos en la fase 1. Las cifras de fallecidos y de infectados por el coronavirus están bajando a números con los que el sistema sanitario puede lidiar con cierta normalidad. Sin embargo, no hay que bajar la guardia, o volveremos a la casilla de salida. El coronavirus se ha cebado con las personas más vulnerables, de edad avanzada o con patologías previas, pero también ha afectado a cierto número de jóvenes sanos. Enrique, ¿se sabe por qué ellos también son vulnerables al coronavirus?
ENRIQUE: La mayoría de las personas que han fallecido presentaban patología previas, como problemas respiratorios, enfermedades cardiovasculares, diabetes u obesidad. En España el 86 % de los fallecidos eran mayores de 70 años, y casi el 60 % eran hombres. Pero no debemos olvidar que más de 100 fallecidos eran menores de 39 años y una decena eran menores de 19 años. De hecho, la Organización Mundial de la Salud ha avisado de que “hay un número significativo de jóvenes que han fallecido”. No sabemos por qué algunos pacientes jóvenes y saludables enferman con síntomas severos y drásticas consecuencias. Tampoco sabemos por qué hay una mayor proporción de fallecimientos en hombres que en mujeres. Ni siquiera por qué algunas personas cursan la enfermedad de forma asintomática.
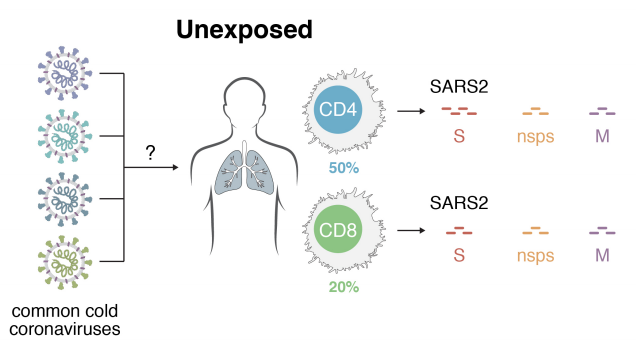
LOLA: Se ha publicado en algunos medios que cuatro de cada diez personas pueden tener inmunidad previa frente al coronavirus, generada por exposición a otros patógenos, lo que podría explicar que haya tantos casos asintomáticos. Francis, ¿qué se sabe sobre este tema?
FRANCIS: Se han publicado esta semana dos artículos, uno en la prestigiosa revista Cell y otro aún en proceso de revisión por pares, sobre el papel de la llamada inmunidad cruzada para explicar los casos asintomáticos. Nuestro sistema inmune dispone de varios tipos de células, entre ellas los linfocitos. Hay dos tipos básicos, los linfocitos T, que reconocen a los virus o son capaces de degradarlos, y los linfocitos B, que producen anticuerpos que bloquean la infección. Los linfocitos T pueden inducir la producción de linfocitos B. Así, los dos nuevos artículos apuntan a que los linfocitos T producidos tras haber sido infectado por un coronavirus, como los que producen un resfriado, pueden activar la producción de linfocitos B contra otro coronavirus, como el que produce la COVID-19. Luego haber pasado uno o varios resfriados podría ayudar al sistema inmune a responder de forma rápida y eficaz contra la COVID-19, explicando los casos asintomáticos. Pero se necesitan más estudios independientes para confirmar los resultados sobre inmunidad cruzada de estos dos artículos científicos.
IGNACIO: Que los hombres fallezcan más que las mujeres podría indicar que hay alguna relación entre la genética y la gravedad de la enfermedad COVID-19. Enrique, ¿podrían tener nuestros genes algún papel en cómo responde nuestro cuerpo a la infección?
ENRIQUE: Así es, hay diferencias en el genoma de cada persona que podrían influir en la gravedad y desarrollo de la enfermedad. Nuestro ADN funciona a modo de libro de instrucciones que hemos heredado la mitad de nuestro padre y la otra mitad de nuestra madre. Un cambio en la cadena de ADN que codifica un gen podría hacer que la proteína generada a partir de este gen funcionara de forma diferente, incrementando la susceptibilidad a la infección por este coronavirus, o produciendo una respuesta del sistema inmune exacerbada ante su presencia.
Por ahora solo se trata de una hipótesis. Muchos especialistas en genética están tratando de identificar los cambios genéticos en las personas más susceptibles, como por ejemplo en las personas jóvenes sin patologías previas que han sufrido una enfermedad muy grave y en algunos casos han tenido un desenlace fatal. Si identificamos los cambios en el ADN de estas personas más susceptibles, se podría aconsejar a estas personas que adoptaran medidas más severas de prevención. Y no solo los genes pueden marcar la diferencia, también hay estudios en marcha sobre un posible papel de la microbiota intestinal en el curso de la infección.

ISABEL: Enrique, esto me llama mucho la atención, porque no estamos hablando de una persona que desarrolla una enfermedad genética porque tiene un cambio en sus genes heredado de sus padres, sino de una respuesta inmune diferente ante la infección por un coronavirus. ¿Sabes si también ocurre con otros virus?
ENRIQUE: Hay muchos estudios previos que han encontrado variantes genéticas en humanos asociadas en la susceptibilidad a ciertas enfermedades producidas por agentes infecciosos: virus (como el del SIDA o de la hepatitis), parásitos (como el de la malaria) o bacterias (como las de la lepra o la tuberculosis). Así, por ejemplo, se han identificado individuos que presentan una resistencia natural al VIH, causante del SIDA. Personas que estaban en un entorno con contacto directo con el VIH pero que nunca enfermaron. Esas personas son un tesoro genético porque pueden tener la clave para una posible cura. Su análisis genético permitió identificar cambios en la secuencia del DNA de un gen llamado CCR5, que codifica una proteína presente en los linfocitos T, que modula la respuesta inflamatoria a la infección, abriendo una puerta al desarrollo de estrategias terapéuticas basadas en inhibidores de la entrada viral.
Tenemos muchos otros ejemplos, pero todavía no sabemos si ocurre algo similar en los afortunados asintomáticos de la COVID-19. Y también ocurre el caso opuesto, mutaciones en genes implicados en las respuestas inmunitarias que hacen que nos defiendan peor ante ciertas infecciones. Así desencadenan una alta susceptibilidad a infecciones por virus o bacterias. Conocer cuál es la causa genética de la mayor susceptibilidad a la COVID-19 tendría muchas aplicaciones, como identificar nuevas dianas para potenciales fármacos y plantear estrategias para disminuir el riesgo de sufrir la infección en las personas portadoras de dichos cambios en su genoma.
FRANCIS: Enrique, por lo que nos cuentas, el posible papel de la genética de una persona en la susceptibilidad a ser infectado por el coronavirus SARS-CoV-2 es un tema de investigación puntera en la actualidad. Hay más de 6600 millones de nucleótidos en la doble hebra de ADN de cada persona, ¿sabes en qué genes concretos se está concentrando este trabajo de identificación de cambios genéticos?
ENRIQUE: Hay varios genes candidatos claros, como el gen ACE2 (en español, ECA2), que codifica para una proteína de membrana (enzima convertidora de la angiotensina) que utiliza el virus SARS-CoV-2 para entrar en la célula. Las variaciones en este gen o en su expresión podrían facilitar o dificultar la entrada del virus en las células. También son candidatos los genes HLA, implicados en la respuesta inmune, que presentan variaciones características en diferentes poblaciones. Estos genes podrían dar mucha información sobre cómo el organismo controla la infección por el coronavirus. Pero la genética suele dar muchas sorpresas y para tener una idea completa es necesario estudiar todo el genoma.
A nivel mundial han surgido más de cien iniciativas públicas y privadas con el objetivo de identificar estas variaciones en el DNA que predisponen a sufrir COVID-19. En España quiero destacar la iniciativa liderada por los investigadores Ángel Carracedo (Grupo de Medicina Genómica de la Universidad de Santiago de Compostela) y Pablo Lapunzina (Centro de Investigación Biomédica en Red de Enfermedades Raras) quienes estudiarán unos 8000 pacientes españoles y latinoamericanos infectados por el SARS-CoV-2. Se espera que la comparación entre los tres grupos en estudio, los asintomáticos, los hospitalizados que no han pasado por la UCI y los que han pasado por ella, revele diferencias estadísticamente significativas que permitan identificar biomarcadores de riesgo.

LOLA: Todos deseamos que estos estudios sean un éxito. Hace solo cinco meses que conocemos la existencia de este nuevo coronavirus y se está avanzando mucho en la comprensión de cómo nos infecta y qué determina cómo evoluciona la infección…
FRANCIS: Y no olvides que el genoma de este coronavirus se secuenció a finales de enero, hace cuatro meses. Nunca se había visto una colaboración tan grande entre grupos de investigación internacionales, tanto públicos como privados. El avance en la comprensión del virus y la enfermedad que provoca requerirá su tiempo, pero lo que debemos tener claro es que la solución para esta pandemia solo puede venir de la mano del conocimiento científico.
ENRIQUE: Y no olvides Francis que la variabilidad de la respuesta de los pacientes a la infección exige una medicina personalizada de precisión. Por desgracia, España es el único país de la Unión Europea sin la especialidad sanitaria de Genética Clínica.
ISABEL: Espero que no por mucho tiempo, Enrique, pero el tiempo apremia y nos tenemos que despedir…

