Gracias a los canales iónicos tu cuerpo siente la temperatura (sentido de la termorrecepción). Se han propuesto varios mecanismos para la activación (apertura/cierre) de los canales iónicos termosensibles de la familia TRP. El más sugerente para un físico es la exposición de residuos hidrófugos al solvente; en dicha hipótesis no existe un único sitio activo donde se localiza el lugar en el que la temperatura activa el canal, sino que esta afecta a la proteína de membrana en su totalidad. Si así se confirma, dado que los canales TRP también son responsables de la sensación de dolor, se complicará mucho el desarrollo de fármacos analgésicos que no influyan en la sensibilidad de este mecanismo de activación por temperatura.
El misterio de la activación por temperatura de los canales iónicos surgió en la discusión posterior a la charla de Teresa Giráldez Fernández (Universidad de La Laguna) en los XV Encuentros con la Ciencia en Málaga, el pasado 15 de diciembre de 2017 [LCMF]. Para un físico la hipótesis más natural es que las vibraciones térmicas del medio actúan como foco de calor que pone a vibrar a la proteína de membrana en su conjunto, facilitando la apertura o cierre del canal. Así que me puse a buscar artículos recientes sobre este tema; me sorprendió la tesis doctoral de Jason Omar Sosa Pagán, «Temperature Activation Mechanism of TRP Ion Channels,» Ph. D. Thesis, Duke University (2017) [PDF], que sigue la línea investigación iniciada por David E. Clapham, Christopher Miller, «A thermodynamic framework for understanding temperature sensing by transient receptor potential (TRP) channels,» PNAS 108: 19492–19497 (2011), doi: 10.1073/pnas.1117485108; sus resultados más relevantes aún no están publicados en revistas (hasta donde he podido explorar). Quizás me ha gustado porque apoya mi hipótesis a priori (sesgo de confirmación); aunque no soy experto en estas lides, me parece un trabajo de investigación a seguir.
Recomiendo el artículo de revisión de Karen Castillo, Ignacio Diaz-Franulic, …, Ramon Latorre, «Thermally-activated TRP channels: Molecular sensors for temperature detection,» Physical Biology (14 Nov 2017), doi: 10.1088/1478-3975/aa9a6f. Sobre la evolución de los canales iónicos, otro tema que surgió tras la charla de Teresa, he encontrado Yang Liu, Fang Lu, …, Yezhong Tang, «Positive selection acted on the extracellular transmembrane linkers of heat receptors during evolution,» Journal of Thermal Biology 64: 86-91 (2017), doi: 10.1016/j.jtherbio.2016.12.004.
Esta entrada participa en la LXV edición terbio del Carnaval de Química, alojada en el blog Quimidicesnews. Anímate a contribuir, tienes hasta el próximo 8 de enero de 2018. Puedes anunciar tu participación por Twitter en @CarnavalQuimica y en @quimidicesnews.
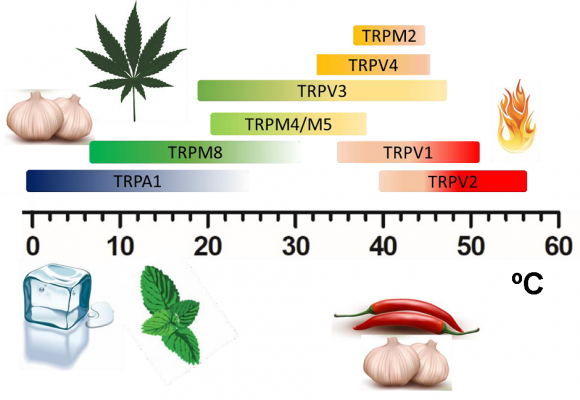
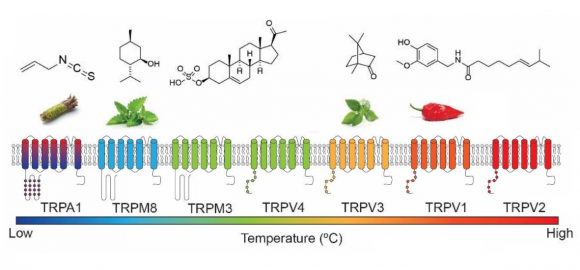
Los organismos vivos necesitan detectar la temperatura para evitar los excesos que pueden provocar daños en sus tejidos, incluso su muerte. Los nocirreceptores (nociceptores) son canales iónicos TRP, siglas en inglés de receptores de potencial transitorio —pésimo nombre cuyo origen es histórico, pues los primeros descubiertos respondían de forma transitoria a la luz—, generan una señal de impulso nervioso (potencial de acción) que a través de las fibras nerviosas llega hasta el sistema nervioso central. Los canales termoTRP son los canales iónicos TRP capaces de detectar la temperatura desde el frío extremo al calor nocivo.
Gracias a las técnicas de criomicroscopía electrónica (Nobel de Química 2017) la estructura tridimensional a escala atómica de muchos canales TRP ha sido desvelada en los últimos años. Bajo la hipótesis de que la estructura determina la función, para algunos de estos canales iónicos se han propuesto mecanismos moleculares detallados de su activación. Sin embargo, para los canales termoTRP aún no se han determinado los dominios responsables de la detección de los cambios de temperatura; o bien es resultado de la acción coordinada de varios dominios, o bien el mecanismo es diferente al de otros canales TRP.
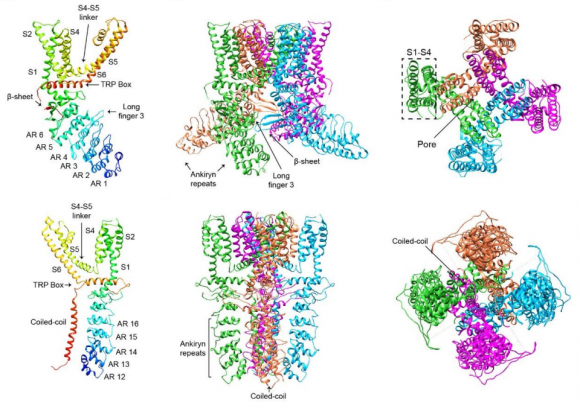
Se han propuesto varios mecanismos para la activación de los canales termoTRP. Una hipótesis es la existencia de una molécula intermediaria; en lugar de que la temperatura active la apertura el canal iónico, lo que produce es la secreción de un mensajero secundario (una molécula como PIP2) que activa el canal. Esta hipótesis tiene el problema de que ciertos canales termoTRP se activan en ausencia de mensajero.
Otra hipótesis es que estos canales responden a los cambios en la tensión mecánica de la membrana celular de fosfolípidos en los que se encuentran insertados; la llamada regulación alostérica inducida por lípidos me parece muy sugerente y estuve hablando de ella con Teresa en Málaga. Sin embargo, algunos estudios apuntan a que la activación se produce incluso sin que medie una membrana de doble capa de fosfolípidos.
Como los canales termoTRP también son sensibles al voltaje (campos eléctricos) y se ha observado que la temperatura afecta a dicha sensibilidad, se ha propuesto que el voltaje es mediador de su sensibilidad térmica; en esta hipótesis la temperatura induce un cambio de voltaje en el canal que permite su activación. Por desgracia, varios estudios apuntan a que una sensibilidad independiente a la temperatura, al voltaje y a señales químicas; en apariencia su única relación es resultado de un efecto colateral.
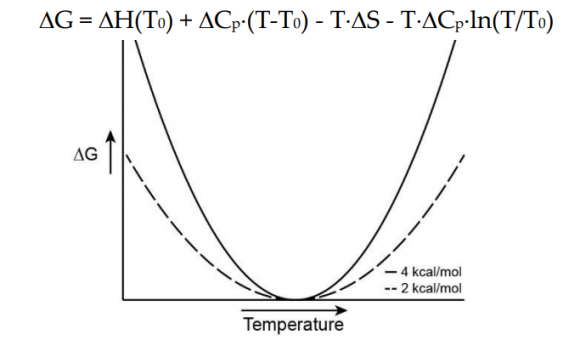
La hipótesis que me parece más interesante como físico fue introducida por Clapham y Miller en 2011; de hecho, su reivindicación por Sosa Pagán ha dado lugar a esta entrada. La capacidad calorífica Cp (el cociente entre la cantidad de energía transferida a la molécula y el cambio de temperatura a la que está sometida) podría dar lugar a pequeños cambios en la conformación (estructura tridimensional) del canal; un cambio ΔCp debido a una modificación de la temperatura del baño térmico al que está sometida la molécula transfiere cierta energía interna y transporta cierta entalpía a su estructura que modifica la energía de activación del canal —recuerda el famoso dictum, la energía interna se transfiere mientras que la entalpía se transporta—.
Este mecanismo termodinámico de activación inducida por la temperatura del canal termoTRP parece muy natural para un físico (y para un ingeniero), aunque quizás no sea del gusto de la mayoría de los biólogos. La razón es que no se puede verificar de forma sencilla usando mutantes —la herramienta básica del biólogo para estudiar sitios activos es modificar la parte de los genes en que se encuentran y comprobar que la proteína mutante deja de funcionar de forma apropiada—. El estudio de este mecanismo requiere conocer la estructura molecular del canal con una resolución atómica y estudiar su comportamiento en un baño térmico mediante el uso de simulaciones por ordenador; para los físicos y los ingenieros es un camino de más fácil tránsito que para la mayoría de los biólogos.
 La verificación de esta hipótesis por un biólogo requiere un arduo camino que exige combinar múltiples técnicas: el análisis de canales quiméricos, la mutagénesis aleatoria, el cribado de alto rendimiento (high-throughput screening), la secuenciación masivamente paralela y, como no, el análisis de múltiples mutaciones puntuales. Por ejemplo, usando las dos primeras técnicas se ha dilucidado que hay residuos en la parte exterior de estas moléculas que son termosensibles, por ejemplo, para
La verificación de esta hipótesis por un biólogo requiere un arduo camino que exige combinar múltiples técnicas: el análisis de canales quiméricos, la mutagénesis aleatoria, el cribado de alto rendimiento (high-throughput screening), la secuenciación masivamente paralela y, como no, el análisis de múltiples mutaciones puntuales. Por ejemplo, usando las dos primeras técnicas se ha dilucidado que hay residuos en la parte exterior de estas moléculas que son termosensibles, por ejemplo, para
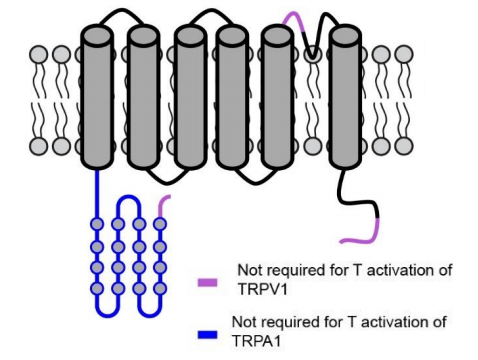
TRPV1 los residuos N628, N652 y Y653, para TRPV3 los residuos I644, N647 y Y661, y para TRPA1 el residuo G878, todos ellos coloreados en la figura; además se han observado cambios en algunos aminoácidos, por ejemplo, para TRPV1 en A657 y Y653, y para TRPV3 en I652 y L655. También se ha observado que el dominio N-terminal (en naranja en la figura) también está relacionado con la activación térmica de TRPA1.
El problema con todos los dominios descritos es que ninguno es suficiente de forma individual para la activación térmica. La eliminación (deleción) de dichos dominios en mutantes no impide que el canal termoTRP siga siendo sensible a la temperatura; incluso la deleción completa del dominio N-terminal de TRPA1 (azul en la figura) o del C-terminal en TRPV1 (morado en la figura). Las versiones truncadas de los canales termoTRP retienen su activación gracias a la temperatura, algo que supone todo un reto para los biólogos estructurales.
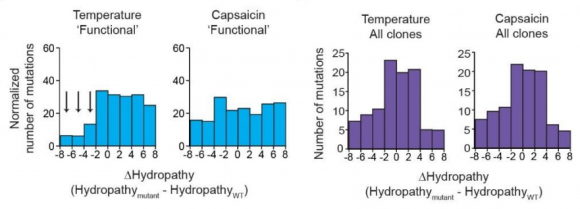
Mediante un estudio basado en ~7300 clones sometidos a múltiples mutaciones aleatorias se ha observado que las que son funcionales para la sensibilidad a la temperatura son las que preservan o incrementan el índice de hidropatía (que mide lo hidrófugo que es un aminoácido). Aplicando el mismo método a un canal iónico activado por la capsaicina resulta que el índice de hidropatía no está correlacionado con su sensibilidad. Los resultados apoyan que ΔCp (un cambio en la capacidad calorífica) sea el mecanismo de la sensibilidad a la temperatura en el canal estudiado y, por ende, que pueda serlo en otros canales termoTRP similares.
Por supuesto, como siempre, se requieren futuros estudios en esta línea. Las técnicas de secuenciación masiva en paralelo permiten análisis de mutaciones aleatorias en toda la proteína que hace un lustro parecían inabordables. Gracias a estas técnicaas el mecanismo que subyace a la sensibilidad a la temperatura es un misterio que promete ser resuelto en el próximo lustro. Quizás la hipótesis termodinámica acabe siendo ratificada, muy al gusto de físicos e ingenieros, o quizás descartada, más al gusto de biólogos y farmacólogos. En cualquier caso acabaremos entendiendo cómo nos duelen el frío y el calor.



Perdona el offtopic: Subiras algo sobre AlphaZero? 🙂 un saludo!
Luca, ya hablé en su momento, https://francis.naukas.com/2017/12/09/alpha-go-zero-domina-el-ajedrez/ ; recuerda que AlphaZero es el nuevo nombre de AlphaGo Zero, que se ha cambiado porque ahora juega al ajedrez, al Shogi y al Go, pero no ha cambiado su arquitectura (lo ideal en un combate de ajedrez serio sería el desarrollo de una arquitectura específica, que se podría llamar AlphaChess Zero, que compitiera contra Stockfish en las condiciones usuales de la competición TCEC).
Me sumo a la petición de que subas escribas más sobre AlphaZero , creo que es una muy buena oportunidad para divulgar sobre IA en un terreno bastante fecundo, los frikis del ajedrez, ja ja.
Por cierto, ayer mismo leía este reportaje:
«Pueden soportar como si nada la fractura de un hueso, pero tampoco notan como deberían el calor sobre la piel, lo que les produce más riesgo de sufrir quemaduras.»
http://www.diariovasco.com/sociedad/asombroso-familia-italiana-20171218211313-nt.html
Y me sorprendía la relación entre sentir dolor y percibir la temperatura, esta familia italiana describe precisamente eso, que no sienten dolor pero no perciben bien la sensación de calor.
El término hidrófugo me quema jaja. En biología se usa hidrófobo o hidrofóbico (que no interacciona con el agua) e hidrófilo o hidrofílico (que sí forma enlaces con la molécula de agua)
Daniel, hasta hace poco tiempo el término hidrófobo en el DRAE no permitía su aplicación a sustancias y dicho uso se consideraba como un anglicismo; ahora ya aparece, pero sigue habiendo una diferencia entre hidrófugo y hidrófobo, el primero solo se aplica a sustancias, nunca a personas, mientras que el segundo tiene varias acepciones, siendo aplicable a personas que padecen hidrofobia. En este blog siempre uso hidrófugo, salvo en su acepción biomédica, aunque estoy de acuerdo contigo con que muchos físicos y químicos siguen recurriendo al anglicismo (ahora ya aceptado).
Hay un estudio interesante por dinámica molécular
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5118185/
Especialmente la observación de la separación de los aminoácidos I679 (lower gate, parte intracellular) que se abren y fluctuan al estado abierto, y en estado cerrado se mantienen muy estables
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5118185/figure/F3/
No veo como la respuesta al calor de una proteína pueda ser mediada por una molécula. Hypotheses non fingo, no concibo ninguna hipótesis de cómo puede ser eso. En cambio, se explica elegantemente y razonadamente que la temperatura provoque un cambio conformacional en la proteína. Ahora bien, algunas plantas por evolución han creado moléculas que producen en la boca de los animales que comen sus frutos la sensación de calor, por medio de la capsaicina; de esa forma los disuaden de comerse los frutos. Pero, ¿cómo una molécula puede «imitar» al calor mismo, es decir, cómo puede la capsaicina interaccionar con los recetores de calor, con sus canales TRP, para producir la sensación de calor?