
Por segunda vez este año una mujer logra un Nobel de ciencias. Frances H. Arnold (Caltech, California, EE UU) logra la mitad del galardón por su trabajo en la evolución dirigida de las enzimas, y George P. Smith (Univ. Missouri, Columbia, EE UU) y Sir Gregory P. Winter (MRC Laboratory of Molecular Biology, Cambridge, Reino Unido) se reparten la otra mitad por la tecnología de presentación de péptidos y proteínas en la superficie de los bacteriófagos (phage display, en inglés). Ambas investigaciones muestran cómo la teoría de la evolución puede ser usada en biotecnología para la producción de fármacos, biocombustibles y otras sustancias orgánicas.
La Dra. Arnold desarrolló en 1993 los primeros estudios de evolución dirigida de enzimas (proteínas que catalizan reacciones químicas). Estos métodos permiten fabricar proteínas con un método respetuoso con el medio ambiente, tanto para la industria farmacéutica como para la producción biocombustibles renovables. El Dr. Smith desarrolló en 1985 el método de presentación de bacteriófagos (virus que infectan bacterias) para fabricar nuevas proteínas (que se presentan en su superficie). El Dr. Winter usó este método para la fabricación de anticuerpos, con el objetivo de desarrollar nuevos fármacos. El primer fármaco comercial fabricado con este método es adalimumab, aprobado en 2002 para tratar la artritis reumatoide, psoriasis e inflamaciones del intestino. Hoy en día hay muchos otros fármacos fabricados con estos métodos que se usan para tratar enfermedades tan extendidas como diferentes tipos de cáncer.
El anuncio oficial del premio está en Press Release, la información divulgativa en Popular Science Background, y la información más técnica en Scientific Background. Por cierto, Frances H. Arnold, @FrancesArnold, es la quinta mujer en obtener el Premio Nobel de Química, tras Marie Skłodowska-Curie (1911), Irène Joliot-Curie (1935), Dorothy Crowfoot Hodgkin (1964) y Ada E. Yonath (2009).
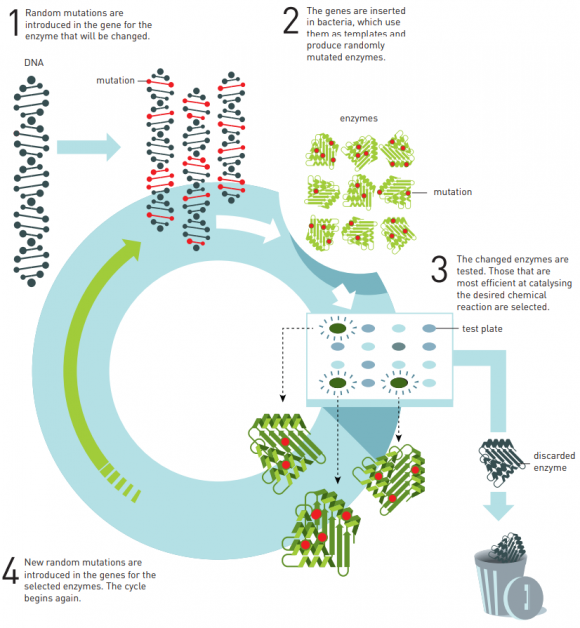
La idea detrás de este Premio Nobel de Química es que para sintetizar ciertas sustancias químicas orgánicas podemos copiar cómo lo hace la Naturaleza tras miles de años de evolución darwiniana. Frances Arnold obtuvo el título de ingeniería mecánica y aeronáutica en 1979, pero decidió orientar su investigación a la síntesis química bioinspirada de sustancias orgánicas, en concreto, enzimas. Las bacterias se pueden usar como fábricas de enzimas (polipéptidos formados por la repetición en cierto orden de los 20 aminoácidos). Pero para ciertas aplicaciones biotecnológicas nos gustaría optimizar las enzimas que existen en la Naturaleza para mejorar su funcionamiento. Para ello podemos usar un proceso iterativo de diseño racional basado en mutagénesis: se introducen mutaciones en el ADN de los genes que codifican las enzimas que queremos mejorar; se fabrican estas enzimas usando bacterias y se realiza un proceso de selección artificial de las mejores para nuestra aplicación; luego se repite el proceso introduciendo nuevas mutaciones en dichas enzimas. Esta evolución dirigida (también llamada evolución in vitro o diseño «irracional») permite optimizar el diseño de las enzimas para su uso biotecnológico.

Los primeros trabajos de Arnold se centraron en la síntesis de la subtilisina (serina endopeptidasa), una proteasa (enzima que digiere otras proteínas). Se obtenía a partir de la bacteria Bacillus subtilis, siendo muy usada en productos comerciales, como detergentes de uso doméstico, cosméticos y procesado de alimentos, y en la síntesis de otros compuestos orgánicos. En un artículo publicado en PNAS, Arnold usó la evolución dirigida para modificar una subtilisina incapaz de romper la caseína (proteína de la leche) para obtener una subtilisina modificada (en 10 aminoácidos) que era 256 veces mejor proteasa contra la caseína (K. Chen, F. H. Arnold, «Tuning the activity of an enzyme for unusual environments: sequential random mutagenesis of subtilisin E for catalysis in dimethylformamide,» PNAS 90: 5618-5622 (1993), doi: https://doi.org/10.1073/pnas.90.12.5618). Su éxito fue emulado y mejorado por otros investigadores que convirtieron esta técnica de síntesis y mejora de proteínas como una herramienta imprescindible en biotecnología. Los trabajos de Arnold se dirigieron a la síntesis de biocombustibles (de gran importancia en la producción de energía renovable), y en otros laboratorios hacia la producción de fármacos (medicamentos). Por lo que su trabajo ha contribuido a un mundo más verde.
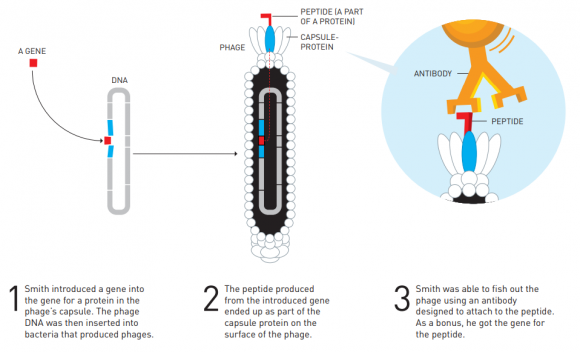 George Smith empezó a usar bacteriófagos en los 1980 para la clonación de genes. Pero en 1985 se dio cuenta de que se podía modificar el genoma de los fagos con nuevos genes que codificaran proteínas (péptidos) de interés biotecnológico, como los anticuerpos (inmunoglobulinas, un tipo de glucoproteína); estas proteínas aparecían en la superficie del fago (G. P. Smith, «Filamentous fusion phage: novel expression vectors that display cloned antigens on the virion surface,» Science 228: 1315-1317 (1985), doi: 10.1126/science.4001944). Esta técnica fue bautizada como presentación de fagos (phage display) ya que la proteína sintentiza se presenta en la superficie del fago, lo que permite su selección y extracción posterior. Ya en 1990 se usó esta técnica para sintetizar nuevas biomoléculas.
George Smith empezó a usar bacteriófagos en los 1980 para la clonación de genes. Pero en 1985 se dio cuenta de que se podía modificar el genoma de los fagos con nuevos genes que codificaran proteínas (péptidos) de interés biotecnológico, como los anticuerpos (inmunoglobulinas, un tipo de glucoproteína); estas proteínas aparecían en la superficie del fago (G. P. Smith, «Filamentous fusion phage: novel expression vectors that display cloned antigens on the virion surface,» Science 228: 1315-1317 (1985), doi: 10.1126/science.4001944). Esta técnica fue bautizada como presentación de fagos (phage display) ya que la proteína sintentiza se presenta en la superficie del fago, lo que permite su selección y extracción posterior. Ya en 1990 se usó esta técnica para sintetizar nuevas biomoléculas.
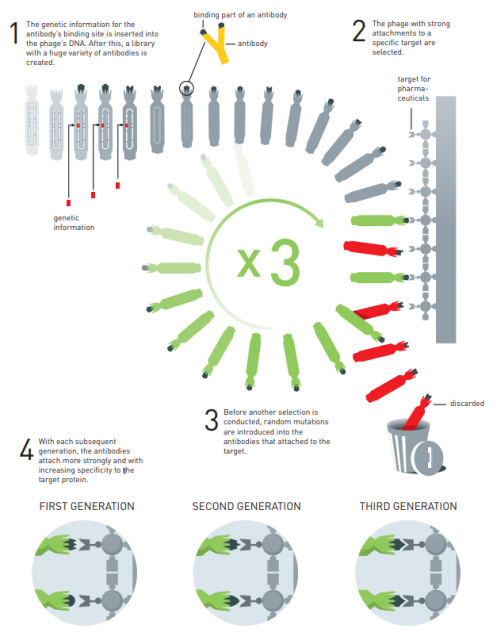
Gregory (Greg) Winter fue de los primeros investigadores que usó la técnica de la presentación de fagos para la fabricación de anticuerpos (moléculas en forma de Y que pueden bloquear muchos procesos bioquímicos asociados a enfermedades). Winter transformó la técnica de la presentación de fagos de Smith en el método más usado para la síntesis de anticuerpos (de hecho, tiene múltiples patentes a su nombre). Ya en 1994 usó este método para fabricar anticuerpos monoclonales que se unen a las células de los tumores cancerígenos (como adalimumab). Estas sustancias se usan en la inmunoterapia oncológica que ha recibido el Premio Nobel de Medicina 2018. Desde 2002 han sido muchos fármacos los que se han fabricado con la técnica de la presentación de fagos para muchas enfermedades. De ahí que las contribuciones de los galardonados con este Nobel de Química son muy relevantes para nuestra sociedad.


OT: http://www.europapress.es/ciencia/astronomia/noticia-mas-pruebas-antartida-particulas-ajenas-modelo-estandar-20181001165212.html
Por favor, que sean partículas de materia oscura.
U-95, no se sabe lo que ha detectado ANITA, pero todo apunta a eventos de fondo. En las primeras observaciones las estimaciones para el fondo siempre son optimistas. Hasta que no se logren nuevas observaciones, que mejoren las estimaciones del fondo, lo más razonable es pensar en señales espurias (que no te engañe la imaginación de los teóricos, que imaginan nuevas partículas por doquier).
Gracias por la respuesta. Lástima, ya me estaba ilusionando con que fuera la puerta a algún nuevos descubrimiento.
Francis
Se pueden en la actualidad diseñar proteinas para uso medico o industrial? Con otras tecnicas que las ganadoras del premio nobel de este año?
Lei lo que se llama proteinas de diseño. eso significa que ya podemos hacer proteinas completamente a diseño?
Crees que es posible que podamos entender el plegamiento de proteinas a partir solo de una cadena de amionacidos?
Hasta que punto el diseño de proteinas llegaremos en los proximos años?
Cecilia, no entendemos la relación entre la función y el plegamiento de una proteína; por ello no podemos diseñar ab initio una proteína para una función concreta. Solo podemos usar el método de prueba y error para mejorar el diseño de una proteína preexistente (que es lo que permiten las técnicas premiadas con el Nobel).
Francis
Me refiero a investigaciones como la del dr baker
https://www.bakerlab.org/
Diseño de proteinas
Como se ve en los dibujos, el mecanismo es el mismo para los dos procesos: «random mutations», «discarded» y selección. Tan simple y tan complicado a la vez