
La transparencia en la investigación científica es clave para la reproducibilidad; un punto clave es la publicación de los software de simulación usados. Buen ejemplo es la polémica desde 2011 entre David Chandler (Univ. California, Berkeley) y Pablo Debenedetti (Univ. Princeton) sobre el segundo punto crítico del agua. Sus grupos de investigación publicaron resultados contradictorios sobre el agua sobreenfriada usando el mismo modelo teórico (ST2). La enconada disputa finalizó en 2018 tras ceder Chandler su código a Debenedetti; resulta que contenía un error. Resuelto el error los resultados coinciden, como cabe esperar (por desgracia, Chandler falleció antes de dar su brazo a torcer).
Las simulaciones del agua por dinámica molecular son difíciles de realizar. Lo habitual es obtener resultados que discrepen según el modelo teórico usado para las interacciones entre moléculas. Aún así, si se usa el mismo modelo teórico los resultados deberían coincidir. Según las simulaciones del grupo de Debenedetti en Princeton publicadas en 2009 existe un punto crítico en el que conviven dos fases (líquida-sólida); según las simulaciones del grupo de Chandler en Berkeley publicadas en 2011 solo existe una única fase (líquida-líquida). Chandler era más prestigioso, así que gran parte de la comunidad se decantó por su resultado.
En 2013 Debenedetti hizo público su propio código y solicitó a Chandler que también lo hiciera, o que al menos le enviara el suyo. Chandler hizo oído sordos a la petición. Pero en 2016 Chandler publicó en Nature una crítica a las simulaciones de Debenedetti, quien aprovechó la oportunidad. Solicitó la mediación de los editores de Nature lo que «obligó» a Chandler a enviarle copia de su código en 2017. Gracias a ello se ha desvelado que el código de Montecarlo de Chandler es más eficiente porque usa una inicialización «secreta» (no documentada en su artículo científico). El grupo de Debenedetti ha demostrado que este «secreto» sesga la simulación y sube la temperatura efectiva de las moléculas, falseando el resultado final. Si se elimina este error resulta que ambos códigos coinciden en sus resultados.
La excusa de Chandler es que tenía recursos ni tiempo para «poner bonito» su código antes de publicarlo; por desgracia, ocultaba un «secreto» no documentado que penalizaba la reproducibilidad y la transparencia que requiere el avance de la ciencia. La publicación de los códigos de simulación debería ser lo habitual. Te recomiendo disfrutar de esta polémica en detalle en Ashley G. Smart, «The war over supercooled water. How a hidden coding error fueled a seven-year dispute between two of condensed matter’s top theorists,» Physics Today (22 Aug 2018), doi: 10.1063/PT.6.1.20180822a. El artículo clave para su solución fue D. Chandler, «Metastability and no criticality,» Nature 531: E1–E2 (2016), doi: 10.1038/nature16539]; el error se ha publicado Jeremy C. Palmer, Amir Haji-Akbari, …, Pablo G. Debenedetti, «Comment on “The putative liquid-liquid transition is a liquid-solid transition in atomistic models of water” [I and II: J. Chem. Phys. 135, 134503 (2011); J. Chem. Phys. 138, 214504 (2013)],» The Journal of Chemical Physics 148: 137101 (2018), doi: 10.1063/1.5029463].
El agua presenta un punto crítico a 374 °C y 218 atm en el que conviven el agua líquida y el vapor de agua. La posibilidad de que haya un segundo punto crítico, en el que conviven el agua líquida y el hilo sólido, aún es un asunto no resuelto. La idea nació en 1976 gracias al trabajo en la Univ. de Purdue de Austen Angell y Robin Speedy con agua superenfriada. Observaron que la compresibilidad isoterma crecía de forma rápida, un signo de que la densidad está fluctuando de forma salvaje a escala molecular entre dos fases. El artículo es R. J. Speedy, C. A. Angell, «Isothermal compressibility of supercooled water and evidence for a thermodynamic singularity at −45°C,» The Journal of Chemical Physics 65: 851 (1976), doi: 10.1063/1.433153. El segundo punto crítico fue propuesto en 1992 por Eugene Stanley (Univ. Boston): Peter H. Poole, Francesco Sciortino, …, H. Eugene Stanley, «Phase behaviour of metastable water;» Nature 360: 324–328 (1992), doi: 10.1038/360324a0. Esta teoría se aceptó como correcta por la mayoría de los expertos: Pablo Debenedetti, Gene Stanley, «Supercooled and Glassy Water,» Physics Today 56: 40 (2003), doi: 10.1063/1.1595053.
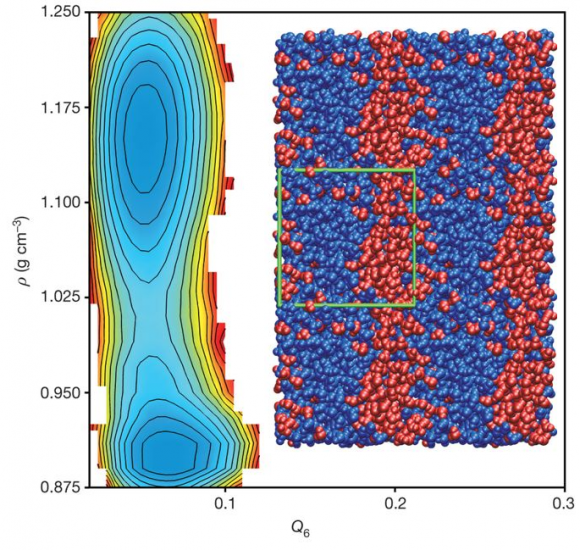
Las limitaciones experimentales requerían el uso de simulaciones por dinámica molecular para estudiar si existe o no existe el segundo punto crítico. El artículo clave que apoyó su existencia es Yang Liu, Athanassios Z. Panagiotopoulos, and Pablo G. Debenedetti, «Low-temperature fluid-phase behavior of ST2 water,» The Journal of Chemical Physics 131: 104508 (2009), doi: 10.1063/1.3229892. Sin embargo, este artículo no era definitivo porque no se calculó el paisaje de la energía libre; lo lograron mucho más tarde, en Jeremy C. Palmer, Fausto Martelli, …, Pablo G. Debenedetti, «Metastable liquid–liquid transition in a molecular model of water,» Nature 510: 385–388 (2014), doi: 10.1038/nature13405 (el resultado que muestro en la figura de arriba es de este artículo).
Las fases termodinámicas de la materia se observan como mínimos (o cuencas de atracción) en el paisaje de la energía libre. Al dibujar la energía libre en función de un parámetro termodinámico (como la densidad) se observa un mínimo si hay una fase y se observan dos mínimos si hay dos fases. . Sin embargo, Chandler, uno de los padres de la teoría del equilibrio de los líquidos de Weeks–Chandler–Andersen, puso en entredicho la existencia del punto crítico en 2011, dando inicio a la polémica. Sus simulaciones por ordenador, realizadas por su estudiante de doctorado Limmer, mostraban un único mínimo de la energía libre, luego había una fase líquido-líquido en lugar de una fase líquido-sólido: David T. Limmer, David Chandler, «The putative liquid-liquid transition is a liquid-solid transition in atomistic models of water,» The Journal of Chemical Physics 135: 134503 (2011), doi: 10.1063/1.3643333.
En todos los congresos donde se presentaban resultados de Chandler o de Debenedetti, había enconadas discusiones en el turno de preguntas. Siendo Chandler más prestigioso, la mayoría de los expertos se decantaban por sus resultados. Más aún, Chandler decía que las simulaciones de Debenedetti eran demasiado cortas, comparadas con las suyas, luego sus resultados estaban sesgados. Debenedetti comprobó y recomprobó sus códigos de simulación (contratando un experto independiente para ello, Palmer); no se encontró ningún error. Por ello empezó a sospechar que las simulaciones de Chandler eran las que contenían algún error. Publicó su código en abierto y solicitó a Chandler que hiciera lo mismo en 2013.

Al final, gracias a la mediación de los editores de Nature, Chandler y Limmer cedieron su código en 2017 a Palmer (ya en Univ. Houston) que buscó errores potenciales. Tras varios meses desveló dónde estaba el error, el truco usado para acelerar el código de las simulaciones de Montecarlo (que no se documentó en el artículo científico). El código de Chandler y Limmer inicializa las posiciones y las velocidades de las moléculas en la simulaciones de dinámica molecular; por desgracia, este proceso sesga los resultados y viola las hipótesis de la mecánica estadística (las energías se desvían respecto a los valores de equilibrio que deben estar gobernados por la distribución de Boltzmann). Como resultado las moléculas en su estado inicial se comportan como si estuvieran una decena de grados más calientes de lo que deberían; el código de Chandler y Limmer estaba realizando las simulaciones por encima del punto crítico; por ello no veían el doble mínimo en el paisaje de la energía libre. Cuando se resolvía esta problema con una inicialización rigurosa, las simulaciones de Berkeley y Princeton coinciden.
El error fue desvelado en un artículo del grupo de Debenedetti publicado en febrero de 2017. Por desgracia, Chandler falleció el 18 de abril de 2017, a los 72 años. Por ello no pudo escribir una respuesta. Aún así, Limmer sigue defendiendo sus simulaciones; pero ahora es el único que las defiende. El resto de la comunidad apoya al grupo de Princeton. Para Debenedetti hay algo positivo en estos 7 años de tiras y aflojas. Los teóricos se han visto forzados a estudiar en más profundidad la metaestabilidad del agua y se ha avanzado en las técnicas de simulación por dinámica molecular. La ciencia siempre gana.
Por cierto, aún se está lejos de resolver el problema del segundo punto crítico del agua. Las técnicas experimentales de difracción con rayos X de alta velocidad permiten estudiar el agua superenfriada en la escala de tiempo de los femtosegundos. Por ahora apoyan la existencia del punto crítico, pero todavía no se ha alcanzado un consenso científico firme. Más información en Kyung Hwan Kim, Alexander Späh, …, Anders Nilsson, «Maxima in the thermodynamic response and correlation functions of deeply supercooled water,» Science 358: 1589-1593 (22 Dec 2017), doi: 10.1126/science.aap8269, y Paola Gallo, H. Eugene Stanley, «Supercooled water reveals its secrets,» Science 358: 1543-1544 (22 Dec 2017), doi: 10.1126/science.aar3575.


Aunque lo expresas muy elegantamente, da toda la impresión de que Chandler hizo trampas. No se sabe si deliberadamente y desde el principio, pero al menos sí lo parece cuando la situación ya estaba más enfrentada.
Y permíteme otra reflexión, sobre la reputación de los científicos, en este caso se daba el crédito al más famoso, pero sus resultados los desarrollara una persona casi desconocida, el alumno de doctorado. Sigue habiendo clases en la ciencia…
Buenas Francisco
No entiendo en qué consiste una transición de fase líquido-líquido.
¿Podrías explicarlo brevemente o citar alguna referencia que lo haga?
Muchas gracias por la respuesta y por el blog en sí.
Así a lo breve:
El agua, incluso en su forma molecular (sin sales) es un ‘elemento’ muy singular. No solo hay que tener en cuenta su polaridad eléctrica, sino también su estructura atómica que dificulta la formación de cristales regulares. Como consecuencia, existen múltiples formas distintas (fases) de ordenar el agua, incluso en su estado líquido. Cada fase tiene sus propiedades termodinámicas y, dependiendo de las condiciones externas, ‘siempre’ habrá una de las fases más estable que las demás, a excepción, claro está, de las transiciones de fase y los puntos críticos.
Gracias espaidual.
De todas maneras, parecee que no me he explicado bien.
Reformulo la pregunta: ¿De qué dos formas se puede ordenar un líquido?
como siempre,
muchas gracias por la entrada. Desconocía por completo éste conflicto.
Solo un apunte: cuando mencionas que el punto critico es «(…) en el que conviven el agua líquida y el vapor de agua». Esta descripción se corresponde a una transición de primer orden. En lenguaje llano yo diría que en el punto critico la separación entre fase ‘líquida’ y ‘gaseosa’ desaparece.
No veo el sentido en buscar un efecto tan esquivo como un segundo punto crítico con un modelo clásico y además rígido del agua. ST2 podría tenerlo y el agua real no, o viceversa.
¿Estamos muy lejos de un ab initio con suficientes moléculas?
(Disclaimer: no simulo agua desde el siglo pasado ?)
Gracias Francis,
Juan Carlos—
@ApuntesCiencia
Me parece que más que un error de software, lo que provocó 7 años de polémica fue la tozudez humana.
Como ingeniero en informática y doctorado en robótica sólo puedo decir que todo el asunto de la calidad del software y lenguajes de programación me da ganas de llorar. Para mí es uno de los elefantes en la sala de los coches autónomos.
Pregunta inocente: ¿Cual es el temor de un investigador de hacer público su código? siempre creí que la filosofía en ciencia era otra. existen otros intereses que ayuden a fomentar estos miedos?
En último término los científicos son trabajadores en un «mercado» con mucha competencia y tratan de maximizar el rendimiento de su esfuerzo. Cuando un código es original y se ha invertido mucho tiempo en desarrollarlo, hay varias filosofías, cuyos dos extremos son: (1) Crear un software abierto o cerrado, gratis o de pago, de uso general, intentando que lo emplee el mayor número posible de personas, ganando citas o bien directamente dinero. (2) Aprovechar durante un tiempo la ventaja que supuestamente proporciona ese programa frente a la competencia, para publicar el mayor número posible de trabajos científicos bien por el grupo desarrollador o en colaboración. En el primer caso, los desarrolladores suelen dedicar esfuerzo a promover y facilitar el acceso al código; en el segundo, suelen ser bastante celosos de que otros tengan acceso a él.
El problema de eso es que no es ciencia, así que te puedes encontrar con una revista seria que se niegue a publicar por falta de reproducibilidad.
Kuhn se pondría las botas con este caso.
«La ciencia avanza con cada funeral»
Daniel, ¿seguro que es una cita de Kuhn? ¿A quién citaba? https://quoteinvestigator.com/2017/09/25/progress/
me hace recuerdo a los “excelsos” y “austeros” Reinhart y Roggoff