
Los libros de texto explican que el agua y el aceite son inmiscibles porque el agua es un compuesto polar, mientras que el aceite es apolar. Sin embargo, cxperimentos a principios del siglo XX mostraron que las gotas de aceite sumergidas en agua presentan un potencial zeta negativo en su superficie, es decir, su superficie está recubierta de cargas negativas (electrones). Hay dos hipótesis para explicarlo: la adsorción de aniones hidróxidos (OH⁻) y la transferencia de carga asociada a la formación de enlaces de hidrógeno C–H···O en la interface. No hay evidencia espectroscópica de la primera; se publica en Science la primera evidencia de la segunda. Se observa una región espectral ancha entre ~2550 a ~2750 cm⁻¹ asociada a la transferencia de carga entre los átomos de oxígeno del agua y los grupos C–H del aceite. Las simulaciones con dinámica molecular confirman que los enlaces de hidrógeno C–H···O pueden explicar la magnitud del potencial zeta observado. Así, el agua y el aceite no se mezclan porque los enlaces de hidrógeno C–H···O son menos fuertes que los enlaces de hidrógeno O–H···O.
Lo más interesante del nuevo artículo es la técnica de medición usada, que promete muchas aplicaciones en metrología. El artículo es Saranya Pullanchery, Sergey Kulik, …, Sylvie Roke, «Charge transfer across C–H⋅⋅⋅O hydrogen bonds stabilizes oil droplets in water,» Science 374: 1366-1370 (09 Dec 2021), doi: https://doi.org/10.1126/science.abj3007.

En los experimentos se han usado nanogotas de hexadecano (C16H34) de 200 nm de diámetro sumergidas en agua pesada pura (D2O); para prepararlas se usan ultrasonidos. Los espectros vibracionales se han determinado usando dispersión por suma de frecuencias (SFS) en la región entre 2200 y 2800 cm⁻¹, para estudiar los enlaces O–D y C–H en la interfaz aceite–agua. Durante las últimas dos décadas se intentó realizar esta medida sin éxito; parecía imposible medir el espectro vibratorio del agua en la superficie de las nanogotas de aceite. Avances recientes han permitido superar dicha limitación, siendo su éxito la contribución del artículo que más impacto tendrá en el futuro; remito a los interesados en estos detalles a consultar la información suplementaria del artículo.
Hay dos grandes diferencias entre los espectros de las interfaces aire–agua y aceite–agua. Por un lado, en la región entre 2395 y 2500 cm⁻¹, donde se observa la fuerza de los enlaces de hidrógeno O–D, siendo más fuertes los que menor amplitud espectral presentan. Como muestra la figura (izquierda) en la interfaz aire–agua los enlaces de hidrógeno O–D son más que en la interfaz aceite–agua. Y por otro lado, un pico centrado en 2745 cm⁻¹ en la interfaz aire–agua, ausente en la interfaz aceite–agua, asociado a grupos O–D que no están ligados por enlaces de hidrógeno (a átomos de H del aceite). Además, se ha estudiado el cambio con la temperatura de la amplitud espectral pico en la región entre 2395 y 2500 cm⁻¹ en la interfaz aire-agua, que crece conforme decrece la temperatura; las medidas extrapoladas indican que la amplitud para la interfaz aceite–agua a 293 K (~20 ºC) es similar a la de la interfaz aire-agua a 277 K (~4 ºC), el punto de congelación del agua pesada (se ha extrapolado porque los espectros no se podían medir en el agua congelada).
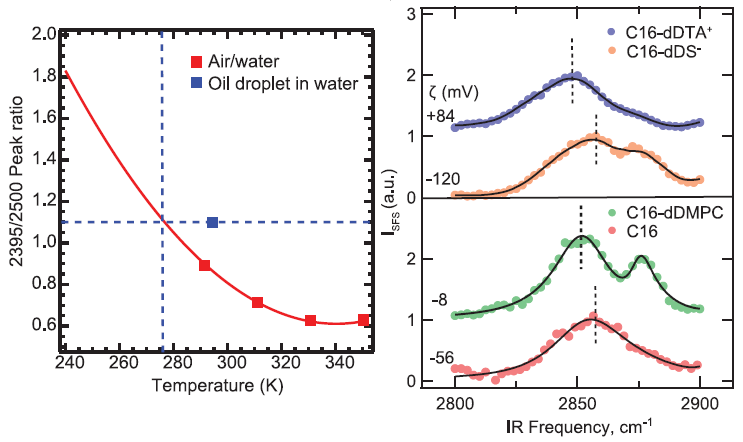
Las simulaciones con dinámica molecular para la interfaz hexadecano–agua muestran un excelente ajuste al espectro observado en la región entre 2395 y 2500 cm⁻¹ (compara la curva en color negro con las observaciones experimentales en color azul). La parte derecha de la figura que abre esta pieza muestra la densidad de probabilidad para el enlace de hidrógeno C–H···O en el plano distancia (Å) versus ángulo (º). Se observa que las moléculas de agua a menos de 5 Å de la interfaz orientan sus átomos de O hacia los grupos CH2 del aceite. Así se concluye que los enlaces de hidrógeno C–H∙∙∙O son responsables de la transferencia de carga entre el agua y el aceite. Estos enlaces ya se habían descubierto hace unos veinte años, pero hasta ahora no se había confirmado su papel en el potencial zeta de –56 ± 10 mV de las gotas de aceite. La adición a las gotas de aceite de una monocapa aislante lipídica de d-DMPC (dimiristoilfosfatidilcolina deuterada) reduce dicho potencial a –8 ± 6 mV, y la adición de una monocapa electronegativa de d-DS⁻ (dodecilsulfato sódico deuterado) incrementa el potencial hasta –120 ± 10 mV.
En resumen, como quizás también te pasara a ti, yo creía que desde hace años se conocía en detalle el origen de la inmiscibilidad del aceite y el agua. Para mi sorpresa, había dos hipótesis en liza, ambas sin apoyo observacional. El nuevo artículo apoya una de estas hipótesis con resultados observacionales y simulaciones numéricas. No sé si los expertos considerarán que la cuestión ya está resuelta, pero al menos parece mucho más cerca de su solución. Como siempre, un último artículo, aunque se publique en Science, nunca es la última palabra en ciencia. Habrá que estar al tanto de cómo reaccionan a este artículo los defensores de la otra hipótesis.


Hola Francis, quisiera hacer una consulta de física elemental a propósito del aceite y del agua. Como sabrás hay freidoras industriales que utilizan aceite y agua para realizar la cocción. El agua queda, por supuesto, en la parte inferior de la cuba del equipo, y generalmente le agrega sal. Por un lado me pregunto cómo pueden funcionar estos aparatos, ya que al aceite se lo calienta a una temperatura de 180ºC, entonces, ¿por qué no hierve el agua bajo el aceite?
Julio, no sabía que existían esas freidoras. En cualquier caso, si hay agua bajo el aceite que no hierve es porque la temperatura del agua se mantiene por debajo de 100 ℃ (la presión ejercida por el aceite es demasiado pequeña para que influya de forma significativa). Para lograrlo hay que calentar el aceite, pongamos a 180 ℃, pero no el agua (basta que haya más aceite que agua y poner la resistencia que calienta el líquido en la zona donde estará el aceite). ¿Por qué el aceite no calienta el agua? Porque se forma un gradiente de temperatura en el aceite, la parte en contacto con la resistencia (que debería estar bajo la posición del recipiente que contiene lo que se fríe) estará a 180 ℃, pero dicha temperatura se reducirá a una temperatura inferior a 100 ℃ en la interfaz con la superficie del agua. Un diseño de este tipo es fácil de concebir y si la freidora alcanza temperaturas mucho mayores (pongamos 250 ℃) basta con incrementar el volumen de aceite y la distancia entre la resistencia y la superficie del agua.
Y ahora a por la explicación detallada de la acción mixta de los jabones con el agua y el aceite a la vez…
Gracias Francis por su respuesta
Hola Francis, a ojos del ignorante (los míos) parece un experimento «fácil» de simular, sin embargo había/hay dos hipótesis candidatas ¿dónde radica la dificultad de predecir/descartar el resultado usando las complejísimas capacidades de simulación disponibles? ¡Gracias!
JoseJuan, tú lo has dicho «parece fácil», pero no lo es. La física cuántica de la interacción de una molécula de agua con un hidrocarburo está más allá de lo que permiten simular los mayores supercomputadores del mundo (necesitamos ordenadores cuánticos para este tipo de cosas). La química cuántica se basa en aproximaciones cuasiclásicas (dinámica molecular, DFT, etc.), que ofrecen respuestas buenas a ciertos problemas (como los cálculos de espectros), pero que en otros ofrecen respuestas que dependen mucho de los parámetros del modelo; se necesitan experimentos que guíen la elección de dichos parámetros, como se ha hecho en este artículo. Las simulaciones computacionales no siempre son útiles para discernir entre hipótesis en liza (ya me gustaría, porque yo investigo en física computacional).
Yo he leído quecse puede añadir un poco de aceite al agua, en frío, antes de calentarla, para que no se peguen los spagetis, y el aceite no salta, no chisporrotea, como cuando vas a freír un filete de pescado o de carne o arroz o pasta cocido/a y escurrido/a, y esta humedo/a; por la diferencia de temperatura.
Por otro lado están también las emulsiones, una mezcla heterogénea, de dos líquidos inmiscibles. En ciertos tipos de magma, glóbulos de ferroníquel líquido pueden estar dispersos dentro de una fase continua de silicato líquido. https://es.m.wikipedia.org/wiki/Emulsi%C3%B3n , diferente a un coloide https://es.sawakinome.com/articles/physical-chemistry/difference-between-colloid-and-emulsion.html
Un saludo.